Эндокринология
- Эндокринологияға арналған препараттар Препараттар
- Эндокринология туралы көбірек оқып біліңіз Туралы көбірек оқып біліңіз
-
ZOMAJET
ZOMAJET
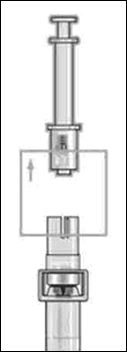
Эндокринология - Инъектор корпусын доза терезесі көрініп тұратындай қылып ұстаңыз
- Айналмалы тұтқасын 1 тілі бағытымен, инъектор түймесінің сыртқа шыққанын естігенше және түймедегі жасыл жолақ көрінгенше бұраңыз.
- 1 тілі бағытымен, доза терезесінде қара жолақ көрінгенше бұрай беріңіз. Инъектор пайдалануға дайын. Назар аударыңыз: Доза терезесінде қара жолақ пайда болғаннан кейін, ары қарай айналмалы тұтқасын бұрамаңыз.
- Айналмалы тұтқасын 2 тілі бағытымен, доза терезесінен «0.00» көрінгенше бұраңыз. Инъектор инесіз бастиекке жалғауға дайын.
- А таңбалы инесіз бастиектің жаңа стерильді қаптамасын ашыңыз. Бастиекті инъекторға жалғау кезінде бастиектің ластану мүмкіндігіне жол бермеу үшін, бастиектің ұшына тиюін болдырмау қажет.
- Бастиектен шығып тұрған шаршы бұдырларын инъектордағы ойықтармен теңестіріңіз.
- Бастиекті инъектор корпусына түбіне дейін жаншып енгізіңіз, бастиектің сақинасы көрініп тұрмауы тиіс.
- Бастиекті солға қарай түбіне дейін бұрыңыз. Егер бастиек дұрыс орнатылса, Сіз аздаған сырт еткен дыбысты сезуіңіз тиіс. Бастиектің шығып тұрған жерлері инъектор корпусындағы белгіленген позицияларға сәйкес келуі тиіс.
- Әрбір бастиекті 7 инъекциядан асырмай немесе бір аптаға есептеп пайдалануға болады және содан соң, инъекция сапалы болуы үшін ауыстырылуы тиіс. ZomaJet 2 Vision және ZomaJet Vision X инъекторларының инесіз бастиектері үш өлшемде қолжетімді: A, B және C. Өзіңіздің алғашқы инъекцияларыңызды А өлшемінен бастаңыз. Жүргізілген әрбір инъекциядан кейін, инъекциялардың сапасын осы нұсқаулықтың "Инъекциялардың сапасына баға беру" бөліміне сәйкес бағалап отырыңыз. Сіз ол бөлімнен Сіз үшін А өлшемін пайдалануды жалғастыра берудің дұрыстығына немесе В өлшеміне көшу керектігіне қатысты нұсқауларды таба аласыз.
- Адаптері бар жаңа қаптаманы ашыңыз.
- Құтының пластик қақпағын алып тастаңыз және резеңке қақпағын спиртпен ысқылап сүртіңіз. Зомактон препаратын өзінің нұсқаулығында сипатталғандай дайындаңыз.
- Адаптерді құтының резеңке қақпағының ортасымен теңестіріңіз және оны «сырт» еткен дыбыс шыққанша орнықтырыңыз. Адаптердің қақпағын алып тастаңыз. Препарат алынғаннан кейін, ары қарай сақтау үшін адаптердің қақпағын жабыңыз.
- Келесі қадамды бастамас бұрын, доза терезесінде «0.00» қойылғанына, ал сақтандырғышының «Жабық» позициясында тұрғанына көз жеткізіңіз. Адаптердің қақпағын алып тастаңыз.
- Инъекторды бастиегін жоғары қаратып тігінен ұстап тұрып, инъектор бастиегінің кедір-бұдырларын құты адаптерінің слотына салыңыз.
- Инъектордың бастиегін адаптерге сырт еткен дыбыс шыққанша енгізіңіз. Бұрамаңыз. Құтының шынысына қолыңызды тигізбеңіз, бұл оның бүлінуне алып келуі мүмкін.
- Инъекторді тігінен ұстап тұрып, айналмалы тұтқасын 2 бағыттағыш бағытымен, доза терезесінде қалаған дозаңыз пайда болғанша бұраңыз.
- Бастиекте ауа көпіршіктерінің бар-жоқтығын тексеріп шығыңыз. Егер Сіз үлкен көпіршіктерді көрсеңіз, олар жоғары көтерілуі үшін инъектордың бастигін жоғары қаратып тігінен ұстап, инъектор бойын түртіп шығыңыз. Көпіршіктер құтыға қарай шығуы үшін, айналмалы тұтқасын 1 бағыттағыш бағытымен жайлап бұраңыз содан соң препаратты қалаған дозаңызға дейін алуды жалғастыра беріңіз.
- Қажетті дозасы алынғаннан кейін, инъекторды бастиегін төмен қаратып аударыңыз, бұл кезде құтыны тегіс жерге қою қажет. Инъекторды құты адаптерінен шығарып алыңыз.
- Сақтандырғышты "АШЫҚ" қалпына аустырыңыз. Инъекторды, бастиегі адамдарға емес, төмен қарап тұратындай қылып ұстаңыз. Инъектор препаратты енгізу үшін дайын.
- санның үстіңгі сыртқы бөлігі;
- кіндік сызығы, немесе кіндіктен бірнеше сантиметр алшақтықтағы орындар;
- бөкселердің үстіңгі сыртқы бөлігі.
- Инъекция орнындағы теріні шымшып жиырмаңыз.
- Инъекция үшін таңдап алынған жерді спиртпен сүртіңіз.
- Стерильді құрғақ бинтті пайдалана отырып, бастиектің ұшындағы сұйықтықты мұқият кетіріңіз
- Сақтандырғышты "АШЫҚ" қалпына ауыстырыңыз. Инъектор разрядтауға дайын және онымен аса сақ болып жұмыс істеу керек.
- Инъекция үшін ыңғайлы позада тұрыңыз. Инъекторды тері беткейіне мықтап тақаңыз. Иньектор иньекция орнына перпендикуляр (90 градус бұрыш жасап) орналасуы тиіс.
- Денеңізді бос ұстаңыз және инъектордың түймесін басыңыз. Түймесін басқан кезде инъекторды жылжытпаңыз. 2 секунд күте тұрыңыз және инъекторды инъекция орнынан алып тастаңыз.
- Көзге көрінетіні: Тері құрғақ болуы тиіс. Тері аздап ылғал болуына болады, бірақ егер сіз сұйықтық тамшысын көрсеңіз немесе инъекция орнынан сұйықтық шығып тұрғанын байқасаңыз, ондай инъекцияны толық емес деп есептеу керек. Аздаған қан тамшысының пайда болуы қалыпты жағдай болып саналады.
- Сезінулер: Сіз өзіңізді жеңіл сезіне аласыз. Егер ауырсыну сезімдері болса, қосымша үйрену немесе кеңес алу үшін өзіңіздің медбикеңізге немесе дәрігеріңізге қоңырау шалыңыз.
-
ЗОМАКТОН
ЗОМАКТОН
(соматропин)
(соматропин)
Эндокринология -
МИНИРИН МЕЛТ
МИНИРИН МЕЛТ
(десмопрессин)
(десмопрессин)
Эндокринология
ZOMAJET
Қазақстан Республикасы
Денсаулық сақтау және әлеуметтік даму
министрлігі Mедициналық және
фармацевтикалық қызметті бақылау комитеті Төрағасының
2017 жылғы “15” 02
№ N 006805 бұйрығымен
БЕКІТІЛГЕН
Медициналық мақсаттағы бұйымды медицинада қолдану жөніндегі нұсқаулық
Медициналық мақсаттағы бұйымның атауы
Өсу гормонын енгізуге арналған ZomaJet 2 Vision / ZomaJet Vision X инесіз инъекторы
Бұйымның құрамы мен сипаттамасы
Инъектор: инъектор корпусы, тексеруге арналған ойық, доза терезесі, айналмалы тұтқа, сақтандырғыш, инъектор түймесі; құтыға кигізілетін адаптер; инесіз бастиек
Қолданылу саласы
Эндокринология
Қолдану тәсілі және дозалары
Инъекция үшін ерітінді дайындауға арналған, еріткішпен жиынтықтағы 4 мг және 10 мг лиофилизацияланған ұнтақ түріндегі Зомактон (ХПА соматропин) өсу гормонын инесіз дозалап енгізуге арналған. ZomaJet 2 Vision инъекторы 4 мг дозадағы Зомактонды, ZomaJet Vision X инъекторы 10 мг дозадағы Зомактонды енгізуге арналған.
Зомактон препаратын ZomaJet 2 Vision және ZomaJet Vision X инесіз инъекторының көмегімен енгізу дозасы мен режимі осы препаратты медициналық қолдану жөніндегі нұсқаулықта сипатталған.
Пациентке инъекцияларды орындау ережелері үйретілуі тиіс!
Инъекторды дайындау
Инесіз бастиекті инъекторға жалғау
Ескертулер:
- Бастиекті 7 инъекциядан артыққа пайдалану жарақат алуға немесе инъектордың кепілдік берілмейтін сынуына алып келуі мүмкін.
- Инъекторға бастиек жалғанбай пайдаланылса және егер бастиек толып тұрмаса, инъектордың кепілдік берілмейтін сынуына алып келуі мүмкін.
- Егер инъектор басқа адамға бағытталып тұрса, оны ешқашан босатпаңыз.
Адаптерді құтыға жалғау
Зомактон салынған әрбір жаңа құты жаңа адаптерді пайдалануды қажет етеді. Адаптер құтыны инъектор бастиегімен жалғау үшін қажет.
Ескертулер:
- Құтының резеңке қақпағын спиртпен сүрту қақпақты тазартады және адаптерді жалғар алдында резеңкені жұмсартуға көмектеседі.
- Адаптерлер тек бір құтымен ғана пайдалануға арналған – адаптерді құтыдан ажыратпаңыз.
- Құты пайдаланылмайтын кезде адаптердің қақпағын жауып қойыңыз.
- Құтыны үнемі тоңазытқышта тік қалпында, 2°С-ден 8°C-ге дейінгі температурада сақтаңыз.
Инъекторды зарядтау
Назар аударыңыз: Егер Сіз байқаусызда Өзіңізге қажетінен көп дозасын алып қойсаңыз, жай ғана айналмалы тұтқасын 1 бағыттағыш бағытымен кері қарай, қалаған дозаңызға дейін бұрыңыз.
Инъекцияны жүргізу
Сіздің дәрігеріңіз немесе медбикеңіз сізге теріасты инъекцияларын жасауды үйретуі тиіс!
Инъекция үшін Сізге дәрігер ұсынған аймақтарды пайдаланыңыз.
Теріасты майы бар орындарды таңдаңыз.
Инъекция үшін ұсынылатын аймақтар:
Инъекцияның сапасын бағалау
Келесі параметрлерді пайдалана отырып, инъекцияның сапасына баға беріңіз. Алғашқы инъекциялардың нәтижелерін «Инъекциялардың нәтижелері» кестесіне жазып қойыңыз.
Егер алғашқы үш инъекцияның екеуі толық болмай шықса, В өлшемді бастиекке көшіңіз. В өлшемді бастиекті пайдалана отырып 3 инъекция жасаңыз. Егер В бастиегіне көшкеннен кейін, сіз инъекциялардың толық болмауына тап бола берсеңіз, Өзіңіздің медбикеңізбен немесе дәрігеріңізге хабарласыңыз.
Айрықша нұсқаулар
Инъектордың жұмысына байланысты кез келген сұрақ туындаған жағдайда, өзіңіздің дәрігеріңізге хабарласыңыз!
Техникалық қызмет көрсету және күтімі
Инъектор техникалық қызмет көрсетуді қажет етпейді. Қабы инъекторды ылғалдан қорғамайды. Инъекторға сұйықтықтың тиюіне жол бермеңіз.
Инъекторды инъекциялар арасында дұрыс сақтау жүйенің дұрыс жұмыс жасауын қамтамасыз ету үшін қажет. Сіз инъекцияны жүргізіп болған соң, айналмалы тұтқасын 1 бағыттағыш бағытымен, түймесі шыққанша бұраңыз, содан соң 2 бағыттағыш бағытымен, доза терезесінде «0.00» пайда болғанша бұраңыз. Содан кейін инъектордың бастиегі мен құтының адаптеріне қорғағыш қақпақтарын кигізіп, инъекторды сақтауға арналған тысына салыңыз.
Ескерту: Инъекторды доза терезесіндегі қара жолағымен немесе қара нүктемен сақтау инъектордың кепілдік берілмейтін сынуына алып келуі мүмкін.
Инъекторды тоңазытқышта сақтауға болмайды.
Сақтау шарттары
Инъекторды бөлме температурасында сақтау керек. Адаптері бар құтыны тоңазытқышта 2 – 8°C температурада сақтау керек.
Жарамдылық мерзімі
Дұрыс жұмыс жасаған жағдайда, пайдаланылу мерзімі шексіз.
Бұл кепілдік модификациялауға, өзгеріске ұшыраған, дұрыс пайдаланылмаған және дұрыс сақталмаған инъекторларға қолданылмайды.
Өндірген
«Antares Pharma Inc,», АҚШ
3905 Annapolis Lane N Suite 105, Minneapolis MN 55447,USA
Ресми дистрибьюторы
Ferring GmbH,Germany
D-24109 Kiel,Germany
\ Ferring International Center SA, Switzerland
Chemin de la Vergognausaz 50,
1162 St-Prex,Switzerland
Қазақстан Республикасы аумағында тұтынушылардан өнім (тауар) сапасына қатысты шағымдарды қабылдайтын және медициналық мақсаттағы бұйымның тіркеуден кейінгі қауіпсіздігін қадағалауға жауапты ұйымның мекенжайы
Қазақстан Республикасындағы «Ферринг Фармацевтикалс С.А.» өкілдігі
Қазақстан Республикасы
Алматы қ., 050059
Әл-Фараби даңғылы, 7
5а блогы, 131 кеңсе
«Нұрлы Тау» бизнес орталығы
Тел.: +7(727) 311 5447, факс: +7(727) 311 5287
ЗОМАКТОН (соматропин)
Қазақстан Республикасы
Денсаулық сақтау және әлеуметтік даму министрлігі
Mедициналық және
фармацевтикалық қызметті
бақылау комитеті Төрағасының
2015 жылғы “12” 11
№ 1220 бұйрығымен
БЕКІТІЛГЕН
Дәрілік затты медициналық қолдану жөніндегі нұсқаулық
ЗОМАКТОН
Саудалық атауы
Зомактон
Халықаралық патенттелмеген атауы
Соматропин
Дәрілік түрі
Инъекция үшін ерітінді дайындауға арналған лиофилизацияланған ұнтақ жиынтықта еріткішпен бірге, 4 мг және 10 мг.
Құрамы
белсенді зат – 4,32 мг (12,96 ХБ) немесе 10 мг (30,00 ХБ) соматропин,
қосымша заттар (4 мг доза үшін): маннитол,
қосымша заттар (10 мг доза үшін): маннитол, натрий гидрофосфат додекагидраты, натрий дигидрофосфат дигидраты,
еріткіш (4 мг доза үшін): натрий хлориді, бензил спирті, инъекцияға арналған су,
еріткіш (10 мг доза үшін): м-крезол, инъекцияға арналған су.
Сипаттамасы
Әсер етуші заты бар 1 ампулада ақ немесе ақ дерлік лиофилизацияланған ұнтақ (4 мг доза үшін); корж түріндегі ақ немесе ақ дерлік лиофилизацияланған ұнтақ (10 мг доза үшін) бар.
Еріткіші бар 1 ампулада мөлдір, түссіз ерітінді бар.
Фармакотерапиялық тобы
Гипоталамустық - гипофизарлы гормондар және олардың аналогтары. Гипофиздің алдыңғы бөлігінің гормондары және олардың аналогтары. Соматропин және оның аналогтары. Соматропин.
АTХ коды H01AC01
Фармакологиялы қасиеттері
Фармакокинетикасы
Тері астына енізгеннен кейін соматропиннің сіңуі 80 % құрайды. Қан плазмасында ең жоғары концентрацияға 3-6 сағаттан соң жетеді және 13-35 нг/мл құрайды. Бауырда метаболизденеді. Жартылай шығарылу кезеңі 3-4 сағатты құрайды. Ішек арқылы шығарылады.
Фармакодинамикасы
Соматропин – Зомактон препаратының белсенді заты амин қышқыл жүйелілігі, құрамы және фармакокинетикалық бейіні бойынша адамның гипофизарлы өсу гормондарына ұқсас полипептид болып табылады.
Зомактон гипофизарлы өсу гормондары тапшы балаларда, түтікті сүйектердің эпифизінің өсу пластинкаларына және сүйек метаболизміне ықпал ете отырып, қаңқа сүйектерінің жалпы пропорционалды түрде өсуіне әсер етеді. Өсу гормоны тапшы және остеопорозы бар науқастарда Зомактонмен орын алмастырып емдеу сүйектердің минералды құрамының және тығыздығының қалыпты болуына әкеледі. Соматропин хондроитинсульфаттың және коллагеннің синтезін белсенді етеді, гидроксипролиннің шығарылуын арттырады. Сарысудың сілтілік фосфотазасының артқаны да байқалады.
Өсу гормонын қолдануға жауап ретінде, жалпы өсуге ұқсас, бұлшық ет жасушаларының саны мен өлшемінің өсуінен қаңқа бұлшықеті өлшемдерінің пропорционалды артқаны байқалады. Сонымен қатар Зомактон басқа тіндерді де арттырады (дәнекер тіндер, тері, айырша без, жасушаларының пролиферациясы жоғары бауыр, жыныс бездерінің, бүйрекүсті бездерінің және қалқанша безінің аздап ұлғаюы). Өсу гормонымен орын алмастыру емі кезінде пропорционалды емес өсу де, жыныстық жетілудің шапшаңдауы да байқалған жоқ.
Зомактон амин қышқылдарының жасушаларға тасымалын және ақуыз синтезін жақсартады, липидтер мен липопротеидтердің бейініне ықпалын тигізе отырып, холестерин деңгейін төмендетеді.
Натрийдің, калийдің және фосфордың кідіруіне мүмкіндік береді. Кальцийдің бүйректер арқылы шығарылуының артуы оның ішекте сіңуінің жоғарылауымен толықтырылады. Осы тұздардың жиналып қалуы олардың тіндердің өсу кезеңінде қажеттілігінің артқанын айғақтайды.
Қолданылуы
- өсу гормонының секрециясының жеткіліксіздігінен өсуі кідірген балаларды емдеуге
- хромосомдық сынама арқылы айғақталған, Тернер синдромына байланысты өсуі кідірген балаларды емдеуге.
Қолдану тәсілдері және дозасы
Зомактон препаратымен емдеу өсу гормоны тапшы пациенттерді емдеу тәжірибесі бар маман дәрігердің бақылауымен жүргізілуге тиіс.
Зомактон дозасын және енгізу тәртібін әр пациенттке жекелей таңдаған жөн.
Әетте емдеу ұзақтығы бірнеше жылды құрайды және ең жоғары қол жеткен емдік әсерге байланысты.
Липоатрофиялардың дамуына жол бермеу үшін енгізілетін жерлерді өзгертіп отырған жөн.
Зомактонмен емдеуді негізгі тиісті дозаларды ескере отырып, бастаған жөн.
Өсу гормоны секрециясының жеткіліксіздігі
Ұсынылатын доза - аптасына әр кг дене салмағына 0,17 – 0,23 мг (4,9 мг/м2 -ден 6,9 мг/м2 –ге дейін дене беткейінің ауданына шаққанда), 6 – 7 теріастылық инъекцияға бөлінген, тиісінше, тәуліктік дозасы әр кг дене салмағына 0,02 – 0,03 мг немесе дене беткейінің ауданына 0,7 – 1,0 мг/м2 құрайды. Жалпы дозаны аптасына 0,27 мг/кг немесе дене беткейінің ауданына 8 мг/м2, сәйкесінше тәуліктік дозаны 0,04 мг/кг асырмау керек.
Тернер синдромы
Ұсынылатын доза – аптасына әр кг дене салмағына 0,33 мг (дене беткейінің ауданына шаққанда шамамен 9,86 мг/м2), 6-7 теріастылық инъекцияға бөлінген, тиісінше, тәуліктік доза әр кг дене салмағына 0,05 мг немесе дене беткейінің ауданына шаққанда 1,40-1,63 мг/м2 құрайды.
Инъекция үшін ерітінді дайындау ережесі (4 мг доза үшін)
Ұнтақты өзінің жанына салынған еріткіште ғана еріткен жөн.
Еріткіштің көлеміне қарай екі концентрация дайындауға болады.
- 3,3 мг/мл концентрациялы ерітінді түзілуі үшін ZOMAJET 2 Vision инесіз иньекторын немесе 1,3 мл еріткіші бар әдеттегідей еккішті пайдаланыңыз,
- 1,3 мг/мл концентрациялы ерітінді түзілуі үшін 3,2 мл еріткіші бар әдеттегідей еккішті пайдаланыңыз.
Ұнтақты тек жанына қоса салынған еріткішпен ғана еріткен жөн.
|
|
1-сурет |
а. Инені бөліктелген еккішке кигізіңіз. б. Құтыдан пластик қақпақты алып тастаңыз. |
|
|
2-сурет |
Ішінде еріткіші бар ампуланың басын сындырып алыңыз, инені ампулаға орналастырар алдында инеден пластик қақпақты алып тастаңыз, еккіштің поршені түбіне дейін тіреліп тұрғанына көз жеткізіңіз. Қажетті еріткішті еккішке баяу құйып алыңыз. |
|
|
3-сурет |
Көпіршіктің түзілуіне жол берму үшін еріткішті құты қабырғасына енгізген жөн. |
|
|
4-сурет |
Ішіндегі ұнтақ мөлдір түссіз ерітінді алынғанға дейін түгел ерігенше құтыны абайлап айналдырған жөн. Шайқамаған немесе қатты араластырмаған жөн. |
Егер ерітінді бұлыңғыр болса немесе онда бөлшектер бар болса, құтыны және оның ішіндегіні жойған жөн. Егер ерітіндінің бұлыңғырлануы салқындағаннан кейін байқалса, онда ерітіндіні бөлме температурасына дейін жылытқан жөн. Егер осыдан кейін ерітінді бұлыңғыр күйінде қалса, құтыны және оның ішіндегісін жою қажет.
Сұйылтқаннан кейін мөлдір түссіз ерітіндіні тері астына, еккішті немесе ZOMAJET 2 Vision инесіз иньекторын қолдана отырып, енгізген жөн. ZOMAJET 2 Vision инесіз иньекторын қолдану жөніндегі брюшора түріндегі нұсқаулық қондырғымен бірге салынған.
Инъекция үшін ерітінді дайындау ережесі (10 мг доза үшін)
Ұнтақты өзінің жанына салынған еріткіште ғана еріткен жөн.
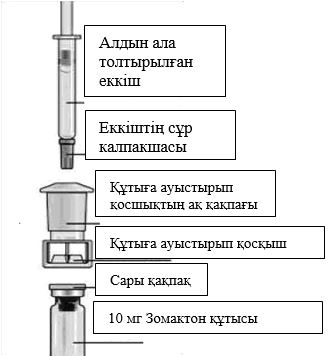
10 мг/мл концентрациялы ерітінді 10 мг Зомактон құтысының ішіндегісін, төменде көрсетілгендей, алдын ала толтырылған еккіш ішіндегі 1 мл еріткіште еріту арқылы дайындалады.
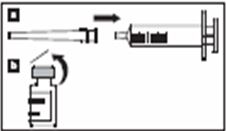
|
|
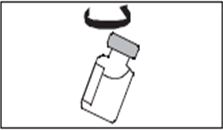
1-сурет |
Қаптамасын ашыңыз және оның ішіндегісімен танысып шығыңыз. |
|
|
2-сурет |
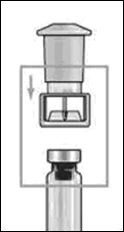
Зомактоны бар құтының сары қақпағын алып тастаңыз. Жалғаманы еккіштің ортасына орналастырыңыз, жалғаманың ұшы төменге қарай бағытталуға тиіс. Осыдан кейін қатты қысыңыз және оны «сырт еткенше» сұғындырыңыз. |
|
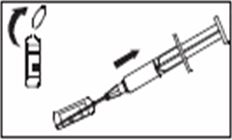
|
3-сурет |
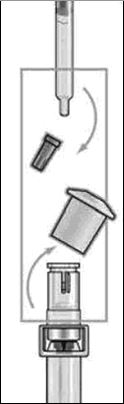
Жалғаманың ақ қақпақшасын және еккіштің сұр қақпақшасын алып тастаңыз. |
|
|
4-сурет |
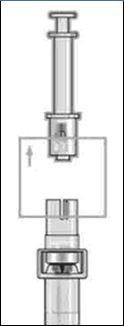
Зомактоны бар құтыны тегіс жерге қойыңыз және оны жалғамасынан ұстай отырып, еккішті жалғамаға орналастырыңыз да, қатты басыңыз. Содан кейін еріткішті құтыға баяу енгізіңіз. |
|
|
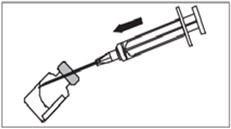
5-сурет |
Зомактоны бар құтыны жалғамасынан ұстай отырып, еккішті алып тастаңыз, жалғама сол жерде қалуға тиіс. Ақ қақпақшаны жалғамаға «сырт еткенше» кигізіңіз. Құтыны ұнтағы түгел ерігенше және мөлдір түссіз ерітінді алынғанша абайлап тербеткен жөн. Шайқауға немесе қатты араластыруға болмайды. |
Жағымсыз әсерлері
Балаларда
Жиі (≥1\1000 <1\10 дейін)
- шеткергі ісінулер, тері бөртпесі, гиперемия, инъекция орнының қышуы
- глюкозаға төзімділіктің бұзылуы
- артралгия, миалгия
Кейде (≥1\1000 <1\100 дейін)
- бұлшықет атрофиясы, сүйектердің ауыруы, карпальді өзекше синдромы, аяқ-қолдағы қимыл шектелуі
Сирек (≥1\10000 <1\1000 дейін)
- гипертензия, ұйқысыздық
- парестезия
Өте сирек (<1\10000)
- лейкемия (алайда оның жиілігі өсу гормонының тапшылығынсыз балаларда байқалатынға ұқсайды)
Ересектерде
Өте сирек (≥1\10)
- бас ауыруы
- шеткергі ісінулер, парестезия, артралгия, миалгия
- жеңіл гипергликемия
Жиі (≥1\1000 <1\10 дейін)
- бас ауыруы, гипертензия, ұйқысыздық
- гипотиреоз
- өсу гормонына антидененің түзілуі (бұл антиденелерді байланыстыратын қабілеті айтарлықтай емес және клиникалық мәні жоқ)
- аяқ-қолдағы қимыл шектелуі
Кейде (≥1\1000 <1\100 дейін)
- ұйқышылдық, нистагм
- гематурия, полиурия, жиі несеп шығару, несеп шығуының бұзылуы
- анемия
- тахикардия, қатерсіз бассүйекішілік гипертензия
- вертиго
- көру жүйкесі дискісінің ісінуі, қосарлана көріну
- абдоминальді ауырулар, іштің кебуі, жүрек айнуы, құсу
Сирек (≥1\10000 <1\1000 дейін)
- диарея
- екінші типті қант диабеті
Өте сирек (<1\10000)
- гинекомастия
Өсу гормонын тері астына енгізу кейде инъекция орнында майлы тіндердің азаюына немесе ұлғаюына әкелуі мүмкін.
Клиникалық зерттеулердің деректері бойынша, балалар жасындағы пациенттердің 2%-да өсу гормонына антидененің түзілгені байқалған. Тернер синдромы бар пациенттердің 8%-ға жуығында өсу гормонының жоғарырақ дозаларын тағайындаған кезде клиникалық зерттеулер кезінде антиденелердің түзілгені байқалған. Бұл антиденелердің байланыстырғыш қабілет төмен болған, және өсу жылдамдығына теріс әсер етуі байқалмаған. Зомактон еміне жауап бермейтін әрбір пациентке өсу гормонына антидененің бар болуына тест жүргізу керек.
Өсу гормонымен ем жүргізілген балалардың біразында лейкемия дамыған. Алайда алдын ала болжанған факторсыз өсу гормонымен ем алған пациенттерде лейкемияның даму жиілігінің артқанына дәлел жоқ.
Ортан жілік басы эпифизінің жылжуы эндокриндік бұзылуымен байланысты, және Легг-Кальве-Пертес синдромы бар балаларда жиі пайда болған. Алайда, бұл аурулар соматропинді қабылдаумен байланысты ма, әлде байланысты емес пе екені белгісіз. Ортан жілікте және тізеде жайсыздық немесе ауырулар болуы мүмкін, бұл нұсқалар қарастырылған.
Басқа да жағымсыз әсерлер, гипергликемия сияқты инсулинге сезімталдық төмендеуі салдарынан, бос тироксиннің бұзылуы, қатерсіз бассүйекішілік гипертензия дамуы мүмкін.
Қлдануға болмайтын жағдайлар
- соматропинге немесе препараттың басқа компоненттеріне аса жоғары сезімталдықта
- түтікше сүйектер эпифиздерінің өсу аймағы жабық балаларда өсуін көтермелеу
- ісік үдерісінің кез келген белгілерінде, қатерлі жаңа түзілімдерде
- жүктілікте және лактация кезеңінде
- шала туған нәрестелерге және жаңа туған нәрестелерге (өйткені 4 мг доза еріткіш құрамында бензил спирті бар)
- ашық кардиохирургиялық, абдоминальды араласымдардан, көптеген жарақаттардан кейін асқынулардан қиын жағдайда болатын пациенттерге, тыныс алудың жедел ағымды жеткіліксіздігінде және осыған ұқсас басқадай жағайларда
- бүйрек трансплантациясында
- белсенді пролиферативті немесе ауыр пролиферативті емес диабеттік ретинопатия
- генетикалық Прадер-Вилли синдромы расталған балаларда өсудің іркілуі
Дәрілермен өзара әрекеттесуі
Препараттардың үйлесімділігі жөнінде деректердің жоқтығын ескеріп, аталған дәрілік затты басқа препаттармен араластырмаған жөн.
Глюкокортикоидтар мен Зомактонды бір мезгілде тағайындаған кезде өсу үдерісіне Зомактонның әсерінің басылғаны байқалады. АКТГ жетіспеушілігі қоса қабаттасқан пациенттер глюкокортикоидтардың мұқият таңдап алынған дозасын қабылдауға тиіс.
Зомактонмен емдеудің тиімділігіне жыныстық стероидты гормондар, анаболикалық стероидтар, гонадотропиндер, тиреоидты гормондар ықпалын тигізеді.
Инсулинмен ем қабылдап жүрген пациенттерде Зомактонды тағайындаған кезде инсулин дозасын түзету қажет болуы мүмкін.
Зомактон P4503A4 цитохромымен метаболизденетін қосылыстардың (жыныстық гормондар, кортикостероидтар, құрысуға қарсы дәрілер және циклоспорин) клиренсін арттырып, осы заттардың қандағы концентрацияларын төмендетеді. Осы өзара әрекеттесулердің клиникалық маңызы белгісіз.
Айрықша нұсқаулар
Зомактонның ең жоғарғы ұсынылатын тәуліктік дозасы арттырылмауы тиіс.
Пациенттерде глюкозаға толеранттылықтың бұзылуын анықтау керек, өйткені өсу гормоны инсулинге төзімділікті туғызуы мүмкін. Зомактонмен емдеу кезінде балаларда глюкозаның қандағы деңгейінің талапқа сай болуын қамтамасыз ету үшін инсулин дозасы арттырылуы мүмкін. Осы пациенттерде глюкозаның қандағы және несептегі деңгейлеріне қатаң бақылау жасалуға тиіс.
Бассүйекішілік зақымданудан болған өсу гормонының тапшылығы бар пациенттерде алдындағы аурудың жағдайына, оның өршуіне немесе кері дамуына мониторинг жасау мақсатқа сай. Зомактонмен емдеуді бірінші жағдайда да, екінші жағдайда да тоқтатқан жөн. Мұның адында қатерлі аурулары болған пациенттерде оның қайталану белгілері мен симптомдарына ерекше назар аударған жөн.
Балалық жастағы онкологиялық ауруларды бастан өткерген пациенттерді соматропинмен емдеген кезде салдарлы қатерсіз немесе қатерлі жаңа түзілімдердің даму қаупі жоғары болғаны (көбіне бассүйекішілік ісігі кездесетіні) байқалған.
Өсу гормонын тағайындаған кезде ісік үдерісі белсенді емес фазада болуы керек және ісікке қарсы ем аяқталуы тиіс. Ісік өсуінің қайта жаңғыру белгілері пайда болса препаратты енгізуді тоқтату керек.
Егер оған өсу гормоны жеткіліксіздігінің диагнозы қатар жүрмесе, Зомактон генетикалық талдаумен расталған Прадер-Вилли синдроммен байланысты, өсуі іркілген балаларды ұзақ емдеуге арналмаған. Педиатриялық іс-тәжірибеде өсу гормонын қолданумен байланысты болған, төменде көрсетілген бір немесе бірнеше қауіп факторы: ауыр семіздік, сыртартқысында көрсетілген тыныс алудың бұзылуы немесе тыныс жолдарының анықталмаған инфекцияларының болуы Прадер-Вилли синдромы бар пациенттерде түнгі апноэ және кенеттен өліп кету жағдайлары жөнінде хабарламалар бар.
Жылдам өсе бастаған кезде кез келген балаларда сколиоз өршуі мүмкін. Соматропинді қолдану кезінде сколиоз белгілерінің пайда болуына бақылау жасаған жөн.
Бүйректерді алмастырып салған кезде Зомактонмен емдеуді тоқтатқан жөн.
Бассүйекішілік қатерсіз гипертензияның сирек жағдайлары болғаны белгілі. Айқын немесе қайталанатын бас ауыру, көрудің нашарлауы, жүректің айнуы/құсу жағдайларында көру жүйкесі дискісінің ісінуін анықтау мақсатында көз түбін зерттеу керек. Көру жүйкесі дискісінің ісінуі айғақталған жағдайда бассүйекішілік қатерсіз гипертензияның бар-жоқтығын қарастырған, ал осы диагноз анықталған жағдайда Зомактонмен емдеуді тоқтатқан жөн.
Гипотиреодты жағдайдың дамуы ықтималдылығын ескеріп, Зомактонды қалқанша без функциясын бақылай отырып қолданады. Соматропинмен емделу кезеңінде T4 гормонының T3 гормонына өтуі белсенді болады, ол T4 плазмалық концентрациясының төмендеуіне және T3 концентрациясының артуына әкеледі. Тұтастай алғанда тиреоидты гормондар деңгейлері қалыпты шекте қалады. Соматропиннің тиреоидты гормондар деңгейіне әсер етуі, генезі орталықтан болатын субклиникалық гипотиреоидты жағдайы бар, гипотиреоз теориялық тұрғыдан дамуы мүмкін пациенттерде клиникалық маңызға ие бола алады. Және керісінше, тироксинмен орын алмастыру емін қабылдап жүрген пациенттерде жеңіл гипертиреоз болуы ықтимал. Сондықтан соматропинмен емдеуді бастаған кезде және оның дозасын таңдағаннан кейін қалқанша без функциясына баға берген мақсатқа сай.
Өсу гормоны тапшы пациенттердің соматропинді қабылдаған да, онымен емделмеген де аздаған бөлігінде лейкемия білінді. 10 жылдық клиникалық бақылаулардың негізінде лейкемия жиілігі өсу гормонының өндірілуі тапшы пациенттерде қауіпті факторлардың жоқтығынан, жалпы популяцияға қарағанда, жоғары болған жоқ.
Эндокриндік бұзылулары бар пациенттерде ортан жілік сүйектерінің эпифизеолизі кездесуі мүмкін. Зомактон қабылдап жүрген, аяғы ақсаңдаған немесе саны немесе тізесі ауыратын пациенттер дәрігерге қаралуы тиіс.
Миозит өте сирек байқалды, ол 10 мг Зомактонға арналған еріткіш құрамында – м-крезолдың болуымен ықтимал. Бұлшықет ауыруы немесе инъекция орны ауырған жағдайда миозитке күдіктенген және ол айғақталған жағдайда Зомактонның м-крезолсыз дәрілік түрін қолданған жөн.
Жүктілік және лактація кезеңі
Зомактонды жүктілік және лактация кезеңінде қолдану жөнінде деректер жоқ. Жануарларға жасалған зерттеулер ұрыққа жағымсыз әсер ететіндігін анықтамады, алайда, соматропинді адамдарға қолданған кезде осыған ұқсас нәтижелер алынады деуге болмайды. Зомактонмен емдеу жүктілік анықталған жағдайда тоқтатылуға тиіс. Жүктілік кезінде ана соматропині елеулі дәрежеде плацентарлы өсу гормонымен орын алмастырады. Соматропиннің ана сүтімен бірге бөлініп шығатын-шықпайтындығы белгісіз, алайда интактілі протеиннің емшектегі нәрестенің асқазан-ішек жолынан сіңуі неғайбыл.
Зомактонның құрамында натрий бар, бірақ дозада 1 ммоль (23 мг) аз натрий, яғни “құрамында натрий жоқ”
Педиатрия
4 мг Зомактон дозасына арналған еріткіш құрамында жаңа туған нәрестелерде және 3 жасқа дейінгі балаларда уытты және анафилактикалық реакцияларды тудыратын бензил спирті бар.
Пациентте панкреатит бар кезде соматропинді абайлап тағайындау керек.
Бұл іштің түйіліп ауыруынан зардап шегіп жүрген балалар үшін өте маңызды.
Көлікті немесе ықтимал қауіпті механизмдерді басқару қабілетіне ықпал ету ерекшеліктері
Жағымсыз әсерлерін ескеріп, сақ болған жөн.
Артық дозалануы
Симптомдары: инициальды гипогликемия, оның артынан гипергликемия келеді. Зомактонның созылмалы артық дозалануы эндогенді өсу гормондары шамадан тыс артық болғандағыға тән симптомдар: алыптық және акромегалия арқылы білінуі мүмкін.
Емі: мұндай жағдайларда препарат қабылдауды тоқтату қажет.
Шығарылу түрі және қаптамасы
Алюминий қалпақшамен қаусырылған және резеңке тығынмен тығындалған, шыны құтыдағы препарат 4 мг немесе 10 мг-ден.
Сындыруға арналған бақылау нүктесі бар түссіз шыныдағы ампуладағы еріткіш 3.5 мл-ден (4 мг доза үшін).
Алдын ала толтырылған еккіште еріткіш 1.0 мл-ден (10 мг доза үшін).
Зомактон 4 мг
а) Ұяшықты қаптамаға дозасы 4 мг және 1 еріткіші бар препаратты 1 құтыдан медициналық қолдану жөніндегі мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге картон қорапқа салынады.
б) Ұяшықты қаптамаға дозасы 4 мг және 1 еріткіші бар препаратты 1 құтыдан медициналық қолдану жөніндегі мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге (Zomajet 2 Vision инесіз инъекторы бар қолдануға арналған жинақ) картон қорапқа салынады.
Зомактон 10 мг
10 мг дозасы және еккішке алдын ала толтырылған 1 еріткіші бар препарат адаптері бар ұяшықты қаптамаға 1 құтыдан медициналық қолдану жөніндегі мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге (Zomajet Vision Х инесіз инъекторы бар қолдануға арналған жинақ) картон қорапқа салынады.
Сақтау шарттары
2°C-ден 8 °C-ге дейінгі температурада түпнұсқалық қаптамасында сақтау керек.
Балалардың қолы жетпейтін жерде сақтау керек!
Сақтау мерзімі
3 жыл
Сұйылтылған препаратты тігінен ұстап тоңазытқышта 2 – 8 °C температурада 14 күннен асырмай (4 мг доза үшін) сақтау керек.
Сұйылтылған препаратты тігінен ұстап тоңазытқышта 2 – 8 °C температурада 28 күннен асырмай (10 мг доза үшін) сақтау керек.
Қаптамасында көрсетілген жарамдылық мерзімі өткеннен кейін пайдалануға болмайды.
Дәріханалардан босатылу шарттары
Рецепт арқылы
Өндіруші
«Вассербургер Арцнаймиттельверк ГмбХ», Германия
Тәркеу куәлігінің иесі
«Ферринг ГмбХ», Германия
Қазақстан Республикасы аумағында тұтынушылардан өнім (тауар) сапасы туралы түскен шағымдарды қабылдайтын ұйымның мекенжайы:
Қазақстан Республикасындағы «Ферринг Фармацевтикалс С.А.» өкілдігі
050059, Қазақстан Республикасы, Алматы қ-сы, әл-Фараби даңғ. 7, 5А блогы, 131 кеңсе, “Нұрлы Тау” БО
Тел./факс.: +7(727) 311-54-47
МИНИРИН МЕЛТ (десмопрессин)
Қазақстан Республикасы
Денсаулық сақтау және
әлеуметтік даму министрлігі
Mедициналық және
фармацевтикалық қызметті
бақылау комитеті Төрағасының
2015 жылғы “08” 10
№ 891 бұйрығымен
БЕКІТІЛГЕН
Дәрілік затты медициналық қолдану жөніндегі нұсқаулық
МИНИРИН МЕЛТ
Саудалық атауы
Минирин МЕЛТ
Халықаралық патенттелмеген атауы
Десмопрессин
Дәрілік түрі
Ішуге арналған лиофилизат, 60 мкг, 120 мкг, 240 мкг
Құрамы
Бір лиофилизаттың құрамында
белсенді зат - десмопрессин ацетаты (десмопрессин негізіне баламалы) 60.00 мкг, 120.00 мкг және 240.00 мкг
қосымша заттар: желатин, маннитол, сусыз лимон қышқылы.
Сипаттамасы
Дөңгелек пішінді, бір жағында жалғыз тамшы түріндегі таңбасы бар (60 мкг доза үшін), ақ түсті лиофилизат.
Дөңгелек пішінді, бір жағында екі тамшы түріндегі таңбасы бар (120 мкг доза үшін), ақ түсті лиофилизат.
Дөңгелек пішінді, бір жағында үш тамшы түріндегі таңбасы бар (240 мкг доза үшін), ақ түсті лиофилизат.
Фармакотерапиялық тобы
Гипоталамды-гипофизарлы гормондар және олардың аналогтары. Гипофиздің артқы бөлігі гормондары. Вазопрессин және оның аналогтары. Десмопрессин.
АТХ коды Н01ВА02
Фармакологиялық қасиеттері
Фармакокинетикасы
Десмопрессиннің биожетімділігі 200, 400 және 800 мкг сублингвальді қабылдауда 0,25 %-ды құрайды (95 % жағдайда сенімді аралығы 0,21-0,31 %-ды құрайды). Қан плазмасындағы ең жоғары концентрациясына препаратты қабылдағаннан кейін 0,5-2,0 сағаттан соң жетеді. Плазмадағы концентрациясы қабылданған дозасының ауқымына тікелей пропорционалды, 200, 400 және 800 мкг қабылдағаннан кейін Смак. сәйкесінше 14, 30 және 65 пг/мл құрайды. Жартылай шығарылу кезеңі 2,8 сағат (СV=24 %).
Десмопрессин гематоэнцефалдық бөгет арқылы өтпейді. Препарат бүйрекпен шығарылады. Тамақпен бір мезгілде қабылдау ас қорыту жолынан сіңірілу деңгейін 40 %-ға дейін төмендетуі мүмкін.
Фармакодинамикасы
Минирин Мелт – вазопрессин молекуласы құрылымындағы өзгерістер –
L-цистеиннің дезаминделуі және 8-L-аргининнің 8-D-аргининге ауысуы нәтижесінде алынған аргинин-вазопрессин табиғи гормонының құрылымдық аналогы. Бұл құрылымдық өзгерістер едәуір күшейтілген антидиуретикалық белсенділікпен біріктірілгенде, вазопрессинмен салыстырғанда, тамырлар мен ішкі мүшелердің тегіс бұлшықетіне болар-болмас әсер етеді, бұл жағымсыз спазмдық әсерлердің болмауына және ұзағырақ әсер етуіне түрткі болады.
Препарат дистальді бөліктің ирек түтікшесі эпителийінің су өткізгіштігін ұлғайтады және оның қайта сіңірілуін арттырады. Препаратты қантсыз диабетте қолдану бөлініп шығатын несеп көлемінің азаюына және бір мезгілде оның осмолярлығының ұлғаюына және қан плазмасының осмолярлығының төмендеуіне алып келеді. Бұл несеп шығару жиілігінің төмендеуіне және никтурияның азаюына әкеп соқтырады.
60-120 мкг препаратты қабылдау көп жағдайда 8-12 сағат бойғы антидиуретикалық әсермен қамтамасыз етеді.
Қолданылуы
- орталық генезді қантсыз диабетте
- алғашқы түнгі энурезді емдеуде
- ересектердегі түнгі полиуриямен байланысты никтурияда (симптоматикалық емдеу)
Қолдану тәсілі және дозалары
Минирин Мелт тіл астына қабылданады. Оңтайлы дозасын жекелей таңдайды.
60 мкг, 120 мкг және 240 мкг Минирин Мелт ішілетін лиофилизаты мен Минирин 0,1 мг және 0,2 мг таблеткаларын дозалау арасындағы арақатынас кестеде келтірілген.
|
Препараттың атауы |
Минирин Мелт |
Минирин |
|
Дәрілік түрі |
Ішілетін лиофилизат |
таблеткалар |
|
Дозасы |
60 мкг |
0,1 мг |
|
|
120 мкг |
0,2 мг |
|
|
240 мкг |
0,4 мг |
Препаратты тамақтанғаннан кейін біраз уақыттан соң қабылдайды, өйткені тамақтану препараттың сіңірілуі мен оның тиімділігіне ықпал етуі мүмкін.
Орталық генезді қантсыз диабет. Дозаны әр емделушіге жекелей анықтайды. Балалар мен ересектер үшін ұсынылатын бастапқы дозасы тіл астына, тәулігіне 3 рет 60 мкг құрайды. Бұдан әрі дозаны емделушінің емдеуге реакциясына байланысты түзетуге болады. Күнделікті дозасы әдетте 120-720 мкг тең. Емделушілердің көпшілігі үшін оңтайлы демеуші дозасы тәулігіне 3 рет 60-120 мкг құрайды. Сұйықтықтың іркілу симптомдары және/немесе гипонатриемия пайда болған жағдайда, емдеуді тоқтату және дозаны түзету қажет.
Алғашқы түнгі энурез. Бүйректің қалыпты концентрациялық қабілеті бар балалар (5 жастан асқан) және ересектер (65 жасқа дейін): ұсынылатын бастапқы дозасы - ұйықтар алдында 120 мкг, тіл астына. Әсері жеткіліксіз болған жағдайда дозасы 240 мкг-ге дейін арттырылуы мүмкін. Емдеу барысында түнгі уақытта сұйықтық қабылдауды шектеу қажет. Сұйықтықтың іркілу симптомдары және/немесе гипонатриемия (бас ауруы, жүрек айнуы/құсу, дене салмағының артуы, құрысулар) пайда болған жағдайда емделушінің жағдайы қалыпқа түскенше, емдеуді тоқтата тұру керек.
Ұсынылатын емдеу ұзақтығы 3 ай, одан кейін 1 аптадан соң қайталау курсын жүргізудің қажеттілігі бағаланады.
Ересектердегі түнгі полиурияға байланысты никтурия (симптоматикалық емдеу). Ұсынылатын бастапқы дозасы – ұйықтар алдында 60 мкг, тіл астына. Бірінші аптада тиімділігі жеткіліксіз болған жағдайда, дозасын 120 мкг дейін және ары қарай қажетінше 240 мкг дейін арттырады. Дозасын арттыруды 1 апта аралықпен жүргізу керек. Емдеу барысында түнгі уақытта сұйықтық қабылдауды шектеу қажет.
Никтуриясы бар емделушілерде емді бастағанға дейін несеп шығарудың жиілігі мен көлемін кем дегенде 48 сағат ішінде бағалаған жөн. Қуықтың функционалдық сыйымдылығынан асып түсетін немесе тәуліктік диурездің 1/3 құрайтын түнгі уақыттағы несеп шығару түнгі полиурия деп саналады.
Қосымша, сарысулық натрий деңгейін емдеуді бастар алдында анықтаған жөн.
Дене салмағын емдеудің басында бірнеше күн бойы және дозаны жоғарылатқаннан кейін тексеру керек. Бір мезгілде тамақтану десмопрессиннің төменгі дозаларында антидиурездік әсерінің қарқындылығы мен ұзақтығын төмендетуі мүмкін.
Егде емделушілерді емдеу ұсынылмайды. Егер оған қарамастан ем жүргізу қажет болса, емдеудің алдында, емдеуді бастағаннан кейін 3 күннен соң, дозаны арттырғаннан кейін 3 күннен соң, сондай-ақ басқа қажетті уақытша нүктелерде сарысулық натрий деңгейін анықтау қажет.
Сұйықтықтың іркілу симптомдары және/немесе гипонатриемия пайда болғанда (бас ауруы, жүрек айнуы/құсу, дене салмағының артуы, құрысулар) емделушінің жағдайы қалыпқа түскенше, емдеуді тоқтата тұру керек. Емдеуді жаңартқаннан кейін емделушілерге сұйық ішуді шектеуді өте мұқият қадағалау және сарысулық натрий деңгейін бағалау керек.
Егер бір апта тиісті дозасын қабылдағанда талапқа сай клиникалық әсері болмаса, емдеуді тоқтату керек.
Жағымсыз әсерлері
Сұйықтық қабылдауды шектеусіз қатарлас емдеу қатар жүретін алдын ала симптомдары бар немесе онсыз организмде сұйықтықтың іркілуіне және/немесе гипонатриемияға (бас ауыруы, жүрек айну/құсу, салмақтың артуы және күрделі жағдайларда, кейде ұзақ уақыт естен тануға дейінгі ұйқышылдықпен байланысты түйілулер) әкелуі мүмкін. Бұл атап айтқанда, бір жасқа дейінгі кішкентай балаларға немесе жалпы жай-күйіне тәуелді болатын егде емделушілерге қолданылады.
Жиі
- бас ауыру, бас айналу
- ауыздың құрғауы, іштің ауыруы, жүрек айнуы, құсу, диарея
- перифериялық ісінулер
- дене салмағының артуы
- ұйқысыздық
- артериялық гипертензия
- поллакиурия
- қажу, шеткергі ісіну
Сирек
- аллергиялық тері реакциялары, жалпы аллергиялық реакциялары
- гипонатриемия
- балалардағы эмоционалдық бұзылыстар
- құрысулар
Қолдануға болмайтын жағдайлар
- десмопрессинге немесе препараттың басқа компоненттеріне аса жоғары сезімталдық
- туа біткен немесе психогендік полидипсия (несеп түзілу көлемі 24 сағатта 40 мл/кг артық), маскүнемдік
- этиологиясы әртүрлі ісінулер
- жүрек жеткіліксіздігі және несеп айдайтын препараттар тағайындауды қажет ететін басқа жағдайлар. Минирин Мелт артериялық қысым деңгейі қалыпты емделушілерде ғана пайдаланылуы тиіс.
- гипонатриемия
- бүйрек жеткіліксіздігі (креатинин клиренсі минутына 50 мл төмен)
- антидиуретиктік гормонның қалыптан тыс секреция синдромы
- 5 жасқа дейінгі балаларға (қантсыз диабет және бастапқы түнгі энурез)
- 65 жастағы және одан асқан емделушілерде десмопрессин никтурия мен алғашқы түнгі энурезді емдеуде пайдаланылғанда
Дәрілермен өзара әрекеттесуі
Үшциклді антидепрессанттар, серотонинді кері қармау селективті тежегіштері, хлорпромазин, карбамазепин және индометацин сияқты әсері антидиуретиктік гормонның қалыптан тыс секреция синдромы дамуын көтермелеуі мүмкін заттар препараттың антидиуретиктік әсерін күшейтуі және организмде сұйықтықтың іркілуі мен гипонатриемия қаупін арттыруы мүмкін.
Қабынуға қарсы стероидты емес препараттар организмде сұйықтық іркілуін / гипонатриемияны индукциялауы мүмкін.
Лоперамидпен қатар емдеу қан плазмасында десмопрессин концентрациясын 3 есе арттыруы мүмкін, бұл сұйықтық іркілуі және гипонатриемиямен байланысты жағымсыз әсерлерінің туындау қаупін арттыруы ықтимал. Ішек тегіс бұлшықеттерінің тонусы мен моторикасын төмендететін дәрілік препараттардың да осындай әсері болуы ықтимал.
Десмопрессиннің бауыр метаболизміне әсер ететін заттармен өзара әрекеттесу мүмкіндігі аз, өйткені десмопрессин адам микросомаларына зертханалық зерттеулерде бауырда қандай да бір елеулі метаболизмге ұшырамайды. Табиғи жағдайларда мүмкін болатын өзара әрекеттесулер бойынша зерттеулер әлі де жүргізілмеген.
Майлары 27% стандартты емдәм ішке қабылданған (мөлшері және ұзақтығы) десмопрессиннің сіңуін едәуір төмендетеді.
Фармакодинамикалық сипаттамасына қатысты (несеп бөлінуі немесе осмоляльдігі), ешқандай елеулі әсері хабарланбаған. Десмопрессин төменгі дозаларында бір мезгілде тамақтану диурезге қарсы әсерінің тиімділігі мен ұзақтығын төмендетуі мүмкін.
Окситоцинді қатар пайдаланған жағдайда диурезге қарсы әсерінің жоғарылуы және жатыр перфузиясының төмендейтінін ескерген жөн.
Клофибрат, индометацин және карбамазепин десмопрессиннің диурезге қарсы әсерін күшейтуі мүмкін, ал глибенкламид оны төмендетеді.
Препаратты диметиконмен бірге қабылдау десмопрессиннің сіңірілуінің азаюына алып келуі мүмкін.
Айрықша нұсқаулар
Алғашқы түнгі энурез және никтурияны емдеу аясында сұйықтық қабылдауды ең аз шамаға шейін, енгізер алдындағы бір сағаттан келесі күнгі таңға дейін қысқарту керек (енгізгеннен кейін кем дегенде 8 сағаттың ішінде). Сұйықтық қабылдауды шектеусіз қатарлас емдеу қатар жүретін алдын ала симптомдары бар немесе онсыз организмде сұйықтықтың іркілуіне және/немесе гипонатриемияға (бас ауыруы, жүрек айну/құсу, салмақтың артуы) және ауыр жағдайларда естен тануға дейінгі сананың тұмандануы болатын ми ісінуіне әкелуі мүмкін. Десмопрессин бүйрек жеткіліксіздігі және/немесе жүрек-қантамыр аурулары, қуық фиброзы кезінде сақтықпен пайдаланылуы керек. Бүйректің созылмалы аурулары кезінде препараттың диурезге қарсы әсері әдеттегіден аздау болады. Қуық функциясының күрделі бұзылуы мен қуық мойны контрактурасы емдер алдында жоққа шығарылуы тиіс.
Егде және сарысулық натий деңгейі төмен емделушілерде гипонатриемия дамуының қаупі жоғары болады.
Су және/немесе су-тұз теңгерімі бұзылуымен сипатталатын аурулардың дамуы жағдайында десмопрессинмен емдеуді тоқтату керек.
Гипонатриемияны болдырмаудың сақтандыру шаралары мына жағдайларда қолданылуы тиіс:
- антидиуретиктік гормонның қалыптан тыс секреция синдромын (SIADH) индукциялауы мүмкін дәрілік заттармен қатар емдеу, мысалы, антидепрессанттар, серотонинді кері қармау селективті тежегіштері, хлорпромазин және карбамазепин;
- қабынуға қарсы стероидты емес препараттармен қатар емдеу.
Сұйықтықпен артық жүктемені болдырмау үшін сақтандыру шаралары мына жағдайларда қолданылуы тиіс:
- электролиттер мен сұйықтық теңгерімі бұзылуының пайда болу қаупі;
- бассүйекішілік қысымның арту қаупі.
Жүктілік және лактация кезеңі
Жүктілікте сақтықпен тағайындайды және артериялық қысым мониторингі ұсынылады. Жүкті әйелдерде болашақ ана үшін күтілетін пайда ұрық үшін ықтимал қауіптен асатын болса ғана, қолдануға болады. Лактация кезінде препаратты тағайындау қажет болған жағдайда, бала емізуді тоқтатады.
Дәрілік заттың көлік құралын немесе қауіптілігі зор механизмдерді басқару қабілетіне әсер ету ерекшеліктері
Жағымсыз әсерлердің болу мүмкіндігін ескере отырып, сақ болу керек.
Артық дозалануы
Симптомдары: организмде сұйықтықтың іркілуі, гипонатриемия, бас ауыру, жүрек айну және ауыр жағдайларда кейде естен тануға дейін сананың тұмандануымен қатар жүретін конвульсиямен судан уыттану.
Емі: дозаны төмендету, бір реттік дозалар арасындағы аралықты ұзарту немесе препарат қабылдауды тоқтату, сұйықтық тұтынуды шектеу және қажет болғанда симптоматикалық ем. Ми ісінуіне күдіктенгенде шұғыл түрде ауруханаға қарқынды ем бөлімшесіне жатқызу қажет болады. Конвульсия да қарқынды шараларды қажет етеді.
Шығарылу түрі мен қаптамасы
10 лиофилизаттан поливинилхлоридті үлбірден және лакталған алюминий фольгадан жасалған пішінді ұяшықты қаптамаға салынған.
3 пішінді қаптамадан медициналық қолдану жөніндегі мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге картон қорапшаға салынады.
Сақтау шарттары
Түпнұсқалық қаптамада, құрғақ жерде, 25 оС-ден аспайтын температурада сақтау керек.
Балалардың қолы жетпейтін жерде сақтау керек!
Сақтау мерзімі
4 жыл
Қаптамасында көрсетілген жарамдылық мерзімі өткеннен кейін пайдалануға болмайды.
Дәріханалардан босатылу шарттары
Рецепт арқылы
Өндіруші
Каталент Ю.К. Свиндон Зидис Лтд, Ұлыбритания
Қаптаушы ұйымның атауы мен елі
Каталент Ю.К. Свиндон Зидис Лтд, Ұлыбритания
Тіркеу куәлігінің иесі
Ферринг Интернешнл Сентер СА, Швейцария
Қазақстан Республикасы аумағында тұтынушылардан өнім (тауар) сапасына қатысты шағымдарды қабылдайтын ұйымның мекенжайы
Қазақстан Республикасындағы «Ферринг Фармацевтикалс С.А.» өкілдігі
Қазақстан Республикасы
Алматы қ., 050059
әл-Фараби д-лы. 7, 5А блок, 131 кеңсе, “Нұрлы Тау” БО
Тел. /факс: +7(727) 311-54-47