Гастроэнтерология
- Гастроэнтерологияға арналған препараттар Препараттар
- Гастроэнтерология туралы көбірек оқып біліңіз Туралы көбірек оқып біліңіз
-
КОРТИМЕНТ
КОРТИМЕНТ
(будесонид)
(будесонид)
Гастроэнтерология -
ПЕНТАСА таблеткалар
ПЕНТАСА таблеткалар
(месалазин)
(месалазин)
Гастроэнтерология -
ПЕНТАСА түйіршіктер 2 г
ПЕНТАСА түйіршіктер 2 г
(месалазин)
(месалазин)
Гастроэнтерология -
ПЕНТАСА ректальді суппозиторийлер
ПЕНТАСА ректальді суппозиторийлер
(месалазин)
(месалазин)
Гастроэнтерология -
ПЕНТАСА ректальді cуспензия
ПЕНТАСА ректальді cуспензия
(месалазин)
(месалазин)
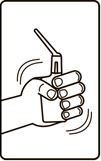
Гастроэнтерология - Тура қолданар алдында алюминий фольгадан жасалған пакеттен құтыны шығарып, жақсылап сілку керек.
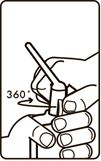
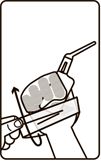
- Тығындалған затты сындыру үшін ұштықты бір толық айналымға бұрау керек (бұраудан кейін ұштық айналдыру алдындағы күйінде болуы тиіс).
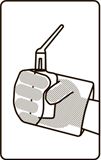
- Қаптамада болатын полиэтилен пакеттердің біреуіне қолыңызды салыңыз.
- Контейнерді пакеттегі суретте көрсетілгендей етіп ұстаңыз.
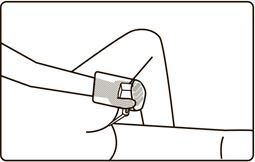
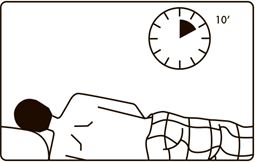
- Клизманы енгізу үшін тепе-теңдік мақсатында сол аяғыңызды тіке, ал оң аяғыңызды алға қарай бүгіп ұстап, сол жақ бүйіріңізге жатыңыз. Аппликатор ұшын тік ішекке абайлап енгізіңіз. Клизма ішіндегі заттың таралуына қарай қолыңызбен барынша тұрақты басып тұрыңыз. Құтының ішіндегісін көп дегенде 30-40 секунд ішінде пайдалану керек.
- Құты босаған бойда оны қысып тұрған күйі құтысымен бірге ұштығын суырып алыңыз.
- Суспензия ішекте қалуы тиіс. Пациент тағы 5-10 минут немесе қысылу басылғанша жоғарыда айтылған қалыпта босаңсыған күйде қалуы тиіс.
- Полиэтилен пакетті бос құтының үстіне қарай сыпырып шешіңіз. Оны тастап, қолыңызды жуыңыз.
-
ПИКОПРЕП
ПИКОПРЕП
(натрий пикосульфаты, магнийдің тотығы)
(натрий пикосульфаты, магнийдің тотығы)
Гастроэнтерология -
РЕМЕСТИП
РЕМЕСТИП
(терлипрессин)
(терлипрессин)
Гастроэнтерология
КОРТИМЕНТ (будесонид)
Қазақстан Республикасы
Денсаулық сақтау министрлігі
Фармация комитеті Төрағасының
2017 жылғы “04” 10
№ N010905 бұйрығымен
БЕКІТІЛГЕН
Дәрілік затты медициналық қолдану жөніндегі нұсқаулық
КОРТИМЕНТ
Саудалық атауы
Кортимент
Халықаралық патенттелмеген атауы
Будесонид
Дәрілік түрі
Босап шығуы ұзаққа созылатын 9 мг таблеткалар
Құрамы
1 таблетканың құрамында:
белсенді зат: 9.00 мг будесонид,
қосымша заттар: стеарин қышқылы, лецитин (соялық), микрокристалды целлюлоза, гидроксипропилцеллюлоза, лактоза моногидраты, сулы коллоидты кремнийдің қостотығы, магний стеараты
үлбірлі қабықтың құрамы: метакрил қышқылының сополимері (А типі), метакрил қышқылының сополимері (В типі), тальк, титанның қостотығы (Е 171), триэтилцитрат
Сипаттамасы
Ақ немесе ақ дерлік түсті үлбірлі қабықпен қапталған, екі жақ беті дөңес, таблетканың бір жақ бетінде «МХ9» өрнегі бар, дөңгелек пішінді таблеткалар.
Фармакотерапиялық тобы
Ас қорыту жолы және зат алмасу. Диареяға қарсы препараттар. Ішектің қабынуына қарсы препараттар. Жергілікті қолдануға арналған глюкокортикостероидтар. Будесонид.
ATХ коды A07ЕA06
Фармакологиялық қасиеттері
Фармакокинетикасы
Сіңірілуі:
Микрондалған қосылыстарды пероральді түрде қабылдағаннан кейін және ол толық сіңгеннен кейін дәрілік заттың ең көп мөлшері шеңберлі ішектің мықын және жоғары көтерілетін бөлімінен сіңіріледі.
Қолданудан кейін 13-14 сағаттан соң қан плазмасындағы будесонидтің ең жоғары концентрациялары шамамен 1,3-1,8 нг/мл құрайды. Будесонидті тамақпен бірге қолдану сіңуіне клиникалық тұрғыдан маңызды әсерін тигізген жоқ. Көп реттік қолданған кезде дәрілік заттың жиналып қалуы мүмкін еместігі көрсетілді.
Таралуы:
Будесонидтің таралу көлемі жоғары (3 л/кг жуық) болады. Қан плазмасы ақуыздарымен байланысуы орта есеппен 85–90% құрайды.
Метаболизмі:
Будесонид бауырда экстенсивті биотрансформацияға ұшырап, глюкокортикоидты белсенділігі төмен метаболиттер түзеді. Негізгі метаболиттердің, 6β-гидроксибудесонидтің және 16α-гидрокси-преднизолонның глюкокортикоидты белсенділігі будесонидтің өз белсенділігінің 1%-нан аспайды. Будесонидтің метаболизмі көбіне Р450 цитохромының туыс тармағы CYP3A изоферменті арқылы болады.
Шығарылуы:
Будесонидтің шығарылу жылдамдығы сіңу дәрежесімен шектеледі. Будесонид жүйелік клиренсінің жоғары екендігін (минутына 1,2 л-ге жуық) көрсетеді.
Педиатриялық популяциялар
Педиатриялық популяцияда фармакокинетикасы жөнінде деректер жоқ.
Фармакодинамикасы
Будесонидтің босап шығуының ұзаққа созылуы дәрілік заттың жаңа инновациялық патенттелген құрамымен: көпматрицалық құрылысымен, рН 7-ден жоғары деңгейде болатын ішек сұйықтығында еритін, асқазан-резистентті қабықпен жабылуымен сипатталады.
Кортиментті қолданғанда таблетканың гастропротекторлық қасиеттері оны асқазан және он екі елі ішек арқылы ішектің төменгі бөлігіне өткен кезде қорғайды. Қорғағыш қабаты еріген кезде ішек сұйықтығы гидрофильді полимерлердің матрицасымен байланысқа түседі, ол гельдің тұтқыр матрицасы түзілгенше ісіне бастайды. Гель матрицасы арқылы өтетін еріткіш әсер ететін затты липофильді матрицалардан босатып шығарады. Будесонид содан кейін, бүкіл жуан ішек бойымен өтуіне қарай, бақыланатын жылдамдықпен ішекке босап шығарылады.
Будесонид ішектің қабыну ауруларын емдегенде пайдаланылатын глюкокортикоид болып табылады. Кортимент қабынуға қарсы жергілікті әсері жоғары глюкокортикоид болып табылады, мұндайда кортизолдың деңгейін кортизолдың деңгейін жүйелік глюкокортикоидтардағы дәрежеде төмендетпейді. Оның глюкокортикоидтық рецепторға аффинділігі гидрокортизонға қарағанда, шамамен 200 есе жоғары, және преднизолонның аффинділігінен шамамен 15 есеге асып түседі.
Қолданылуы
- жеңіл немесе орташа белсенді ойық жаралы колиті бар пациенттерде ремиссия үшін.
Қолдану тәсілі
Ересектер
Ремиссияның индукциясы үшін ұсынылатын тәуліктік доза 8 апта бойы таңертең 9 мг бір таблетканы құрайды.
Кортиментттің 9 мг бір таблеткасын ішке, тамақ ішуге қарамай-ақ, таңертең қабылдайды. Таблетканы шайнамай, ұнтақтамай, сумен ішіп, тұтастай жұтқан жөн.
Препарат қабылдауды күрт тоқтатуға болмайды, дозаны біртіндеп төмендету қажет.
Педиатриялық популяция
Осы дәрілік түр 18 жасқа дейінгі балаларға қолданылмайды. Препаратты балаларда қолдану тәжірибесі шектеулі.
Егде жас
Дозаны түзету қажет емес. Дегенмен, препаратты егде жастағы пациенттерге қолдану тәжірибесі шектеулі.
Бауыр және бүйрек функциясы бұзылған пациенттер
Кортимент 9 мг препараты бауыр және бүйрек функциясы бұзылған пациенттерде зерттелген жоқ, демек, мұндай пациенттерге препаратты қолданғанда және мониторинг жүргізгенде сақтық таныту қажет.
Жағымсыз әсерлері
|
MedDRA (Нормативті-құқықтық қызметтің медициналық сөздігі) бойынша ағзалар жүйесінің класы |
Дұрыс қолдану термині |
||
|
|
Жиі ( ≥1/100-ден <1/10 дейін) |
Жиі емес (≥1/1000-нан <1/100 дейін) |
Сирек (≥1/10 000-нан <1/1000 дейін) |
|
Асқазан-ішек жолы тарапынан бұзылулар |
Жүректің айнуы, жоғарғы бөлімдерінде абдоминальді ауыру |
Іштің кебуі, абдоминальді ауыру, диарея, диспепсия |
|
|
Жүйке жүйесі тарапынан бұзылулар |
Бас ауыру |
Ұйқышылдық |
|
|
Психикалық бұзылыстар |
Ұйқысыздық, көңіл-күйдің өзгеруі |
|
|
|
Тері және теріасты шелі тарапынан аурулар |
|
Безеулер |
Прурит |
|
Жалпы бұзылулар және енгізген жердің бұзылулары |
|
Дәрілік препараттың тиімсіздігі |
Қажығыштық, шеткері ісіну |
|
Бұлшықет-қаңқа жүйесі және дәнекер тіндер тарапынан бұзылулар |
|
Аяқ-қолдың ауыруы |
|
|
Зертханалық зерттеулер |
Қанда кортизол деңгейінің төмендеуі |
|
|
|
Эндокриндік жүйе тарапынан бұзылулар |
|
Кушингоидтық синдром |
|
|
Инфекциялар және инвазиялар |
Тұмау, жоғарғы тыныс жолдарының вирустық инфекциясы |
|
|
|
Қан түзу және лимфалық жүйе тарапынан бұзылулар |
|
Анемия |
|
- сиректеу жүйелік глюкокортикостероидтарға тән жағымсыз әсерлер білінуі мүмкін. Бұл жағымсыз әсерлер дозаға, емдеу ұзақтығына, басқа глюкокортикостероидтармен қатар жүргізілетін немесе мұның алдындағы емге және әркімге жекелей жақпаушылығына байланысты.
Стероидтар класының жағымсыз әсерлері мыналарды қамтиды:
Тері жабындары тарапынан:
- аллергиялық экзантема, қызыл стриялар, петехия, экхимоз, стероидтық акне, жараның баяу жазылуы, жанаспалы дерматит
Бұлшықет-қаңқа жүйесі, дәнекер тіні және сүйектер тарапынан:
- сүйектердің (ортан жілік сүйегінің және иық сүйегі басының) асептикалық некрозы
Көру мүшелері тарапынан:
- глаукома, катаракта
Психикалық бұзылыстар:
-депрессиялық синдром, ашушаңдық, эйфория
Асқазан-ішек жолы тарапынан:
- асқазан тарапынан шағымдар, он екі елі ішек ойық жарасы, панкреатит
Зат алмасудың және тамақтанудың бұзылулары:
Кушинг синдромы, ай тәрізді бет, тұлабойдың семіруі, глюкозаға төзімділіктің төмендеуі, қант диабеті, натрийдің іркіліп, ісінулердің түзілуі, калийдің бөлініп шығуының күшеюі, бүйрекүсті безі қыртысының белсенді болмауы және/немесе атрофиясы, балаларда бойдың өсуінің кідіруі, жыныс гормондары секрециясының бұзылуы (мысалы, аменорея, гирсутизм, импотенция)
Жүрек-қантамыр жүйесі тарапынан:
- гипертензия, тромбоздың жоғары қаупі, васкулит (ұзақ мерзімдік емдеуден кейін тоқтату синдромы)
Иммундық жүйе тарапынан:
- иммундық жауаптың бұзылуы (мысалы, инфекциялар қаупінің ұлғаюы)
Педиатриялық популяция
Деректер жоқ.
Қолдануға болмайтын жағдайлар
- будесонидке немесе препараттың басқа да компоненттеріне аса жоғары сезімталдық
- арахиске немесе сояға жоғары сезімталдық
- галактозаның, фруктозаның тұқым қуалайтын жақпаушылығы; сахараза-изомальтаза тапшылығымен бірге лактаза жеткіліксіздігі, немесе глюкоза-галактоза мальабсорбциясы синдромы
- 18 жасқа дейігні балалар мен жасөспірімдер
Дәрілермен өзара әрекеттесуі
Будесонид жүйелік белсенділігінің аздығын көрсетеді, сондықтан дәрілік өзара әрекеттесулер азаюы мүмкін. Дәрілік өзара әрекеттесулер қаупі ұлғайған пациенттерге егде жастағы адамдар және бүйрек немесе бауыр функциясы бұзылған пациенттер жатады.
Будесонид Р450 3A4 (CYP3A4) цитохромымен метаболизденеді, демек, осы ферменттің тежегіштері, мысалы, кетоконазол, итраконазол, эритромицин және грейпфрут шырыны будесонидтің жүйелік әсерін арттыруы мүмкін. Кетоконазолмен бірге қолдану, жеке будесонидпен салыстырғанда, будесонид концентрациясы - уақыты (AUC) қисығы астындағы ауданның 8 есе артуына әкеледі. Грейпфрут шырынының, ішектің шырышты қабығындағы CYP3A4 тежегішінің көп мөлшерін қолданғанда будесонидтің жүйелік әсері шамамен екі есеге артады. Басқа CYP3A4 белгілі тежегіштерімен емдеу осыған ұқсас әсер береді деп күтіледі. Будесонидтің әсер етуімен CYP3A4 изотүр арқылы басқа дәрілік заттар метаболизмінің тежелуі неғайбыл, өйткені будесонид осы ферментке аффинділігінің төмен екендігін көрсетеді.
Жекелеген пациенттерде едәуір қауіптілік тудыруы мүмкін кортикостероидтармен өзара әрекеттесуге түсетін заттарға жүрек гликозидтері (калий деңгейінің азаюы нәтижесінде әсерінің күшеюі) және диуретиктер (калийдің шығарылуының күшеюі) жатады.
Эстрогендермен немесе пероральді контрацептивтермен бірге қабылдағанда қан плазмасында будесонид деңгейінің жоғарылауы және әйелдерде кортикостероидтар әсерлерінің күшеюі байқалады. Дегенмен, қан плазмасында пероральді преднизолонның концентрациясын екі еседен астамға арттырған біріктірілген төмен дозалы пероральді контрацептив плазмада пероральді будесонидтің концентрациясына елеулі әсерін тигізген жоқ. Құрамында этинилэстрадиол бар ұрықтануға қарсы заттар будесонидтің фармакокинетикасына ықпалын тигізетінін көрсетті.
Зерттеулер жүргізілмегендіктен, холестираминді немесе антацидтерді бірге қолдану басқа дәрілік заттармен қатар, будесонидтің сіңуін азайтуы мүмкін. Демек, мұндай препараттар бір мезгілде емес, ең жоқ дегенде, екі сағат аралықпен қабылдануы тиіс.
Ұсынылған дозаларда омепразол пероральді будесонидтің фармакокинетикасына қандай да болсын ықпалын тигізген жоқ, ал циметидин будесонидтің плазмадағы деңгейінің аздап жоғарылауына әкелуі мүмкін, алайда бұл клиникалық тұрғыдан аздаған әсер ғана.
Айрықша нұсқаулар
Таблетка түріндегі Кортимент препаратын инфекциялары, гипертензиясы, қант диабеті, остеопорозы, асқазанның және он екі елі ішектің ойық жарасы, глаукомасы, немесе глюкокортикоидтарды қолдану жағымсыз әсер беруі мүмкін кез келген басқа жағдайдағы пациенттерге сақтықпен қолдану қажет.
Таблетка түріндегі Кортимент препаратымен емдеу, дәстүрлі пероральді глюкокортикоидпен емдеумен салыстырғанда, стероидтардың азырақ жүйелік деңгейге жеткізілуін қамтамасыз етеді. Басқа стероидтық емнен ауысқан кезде стероидтардың жүйелік деңгейінің өзгеруімен байланысты симптомдар білінуі мүмкін. Жүйелік глюкокортикоидтарды биожетімділігі төмен таблетка түріндегі Кортимент сияқты препараттарға алмастыру бұрын жүйелік дәрілік заттың жәрдемімен бақыланған ринит және экзема сияқты аллергияларды бүркемелеуі мүмкін. Сондай-ақ стероидтарды тоқтатумен астасатын қатерсіз бассүйекішілік гипертензия сияқты басқа да симптомдар пайда болуы мүмкін. Демек, мұндай пациенттерде бүйрекүсті қыртысы қабатының функциясына мониторингті қажет етуі мүмкін, ал жүйелік стероидтардың дозасы сақтықпен төмендетілуі тиіс.
Инфекциялар
Қабыну реакцияларының және иммундық жүйенің басылуы инфекцияларға сезімталдықты және олардың ауырлығын арттырады. Клиникалық көріністер атипиялық болуы мүмкін, ал сепсис және туберкулез сияқты күрделі инфекциялар бүркемеленуі және байқалу сәтіне дейін асқыну сатысына өтіп кетуі мүмкін.
Пероральді глюкокортикоидтарды қабылдап жүрген пациенттерде желшешек және қызылша барысы өте ауыр болуы мүмкін. Осы аурулармен бұрын ауырмаған пациенттерге әсер етуіне жол бермеу үшін аса сақтық таныту қажет. Пациентте инфекцияның бар екендігі байқалғанда немесе күмәнданған жағдайда дозаны төмендету немесе емдеуді тоқтату ықтималдылығын қарастыру және дәрігерден шұғыл түрде кеңес алу қажет. Жүйелік кортикостероидтарды қабылдап жүрген немесе оларды мұның алдында 3 ай бойы пайдаланған, әсерге ұшыраған иммундық емес пациенттерде желшешек (VZIG) иммуноглобулинімен пассивті иммунизация қажет болады, ол желшешек вирусымен жанасудан кейін 10 күн ішінде жүргізілуі тиіс. Желшешек диагнозы айқындалғаннан кейін ауру маманның бақылауымен шұғыл түрде емдеуді қажет етеді. Кортикостероидтарды қолдану тоқтатылмауы тиіс, сондай-ақ доза арттырылуы мүмкін. Қызылшасы бар пациентпен қарым-қатынаста болған, иммундық жүйесі әлсіреген пациенттер тексерілуі тиіс және қажет болғанда иммуноглобулинмен ем қабылдауы керек.
Глюкокортикоидтар гипоталамус-гипофизарлы-бүйрекүсті безі осінің басылуын және күйзеліске реакцияның төмендеуін туындатуы мүмкін. Пациенттер хирургиялық араласымға немесе басқа да күйзеліс әсеріне ұшырған кезде жүйелік глюкокортикоидпен қосымша ем жүргізу ұсынылады.
Бауыр функциясының нашарлауы глюкокортикоидтардың шығарылуына әсерін тигізуі мүмкін. Будесонидті пероральді қабылдаудан кейінгі фармакокинетикасы бауыр функциясы бұзылған кезде өзгереді, мұны орташа ауыр бауыр циррозы бар пациенттерде жүйелік қолжетімділіктің артуы айғақтайды.
Бауыр функциясының бұзылуы ауыр (мысалы, бауыр циррозы бар) пациенттерде жүйелік жағымсыз құбылыстардың даму қаупі ұлғайған.
Емдеуді тоқтату қажет болған кезде дозаны біртіндеп тоқтату қажет. Кейбір пациенттерде препаратты тоқтату кезеңі ішінде спецификалық нашар сезіну, мысалы, бұлшықеттердің және буындардың ауыруы байқалуы мүмкін. Егер сирек жағдайларда қажығыштық, бас ауыру, жүректің айнуы және құсу сияқты симптомдар пайда болса, глюкокортикоидтар әсерінің жалпы жеткіліксіздігіне күдік пайда болуы тиіс. Мұндай жағдайларда жүйелік глюкокортикоидтарды уақытша қолдану қажет етілуі мүмкін. Будесонидтің құрамында болатын басқа препараттар туралы қолжетімді ақпаратқа назар аудара отырып, емдеуді кенеттен тоқтату ұсынылмайды. Препаратты тоқтатудың ықтимал әдісі бір апта ішінде күнара бір таблеткадан қабылдау болуы мүмкін, содан кейін ем тоқтатылуы мүмкін.
Ағымдағы кезеңде немесе пациенттің өзінің немесе алғашқы қатарлы жақын туыстарының кез келгенінің анамнезінде депрессиялық синдром, маниакальді-депрессиялық ауру және мұның алдындағы стероидты психоз сияқты ауыр аффективті күй бар болатын пациенттерде жүйелік кортикостероидтарды қолдану ықтималдылығын қарастырғанда аса сақтық таныту қажет болады.
Әсіресе жоғары дозаларын тағайындаған және ұзақ уақыт бойы қолданған жағдайда стероидтардың жүйелік әсерлері байқалуы мүмкін. Мұндай әсерлер Кушинг синдромын, бүйрекүсті бездерінің супрессиясын, бойдың өсуінің кідіруін, сүйек тінінің минералды тығыздығының төмендеуін, катарактаны, глаукоманы және, өте сирек, психиатриялық/мінез-құлықтық әсерлердің кең ауқымын қамтуы мүмкін.
Кортимент таблеткасының құрамында лактоза моногидраты бар, сондықтан сирек тұқым қуалайтын фруктоза жақпаушылығы, Lapp-лактаза ферментінің тапшылығы, глюкоза мен галактоза мальабсорбциясы сияқты аурулары бар пациенттерге қолдануға болмайды.
In vivo зерттеулер кетоконазолды (бауырда және ішектің шырышты қабығында CYP3A белсенділігінің тежегіші) пероральді будесонидтің жүйелік әсерін бірнеше есеге арттыратындығын көрсетті. Егер будесонидпен бірге кетоконазолмен емдеу көрсетілген болса, жүйелік глюкокортикоидтарға тән жағымсыз әсерлер пайда болған жағдайда будесонидпен емдеуді тоқтату мүмкіндігін қарастыру қажет.
Грейпфрут шырынының (ол көбіне ішектің шырышты қабығында CYP3A белсенділігін тежейді) едәуір мөлшерін қолданудан кейін пероральді будесонидтің жүйелік әсері шамамен екі есеге артты. Көбіне CYP3A арқылы метаболизденетін басқа дәрілік заттардағы жағдай сияқты, грейпфрутты немесе грейпфрут шырынын будесонидпен бір мезгілде үнемі пайдалануға жол бермеу қажет (апельсин шырыны немесе алма шырыны сияқты басқа шырындар CYP3A белсенділігін тежемейді).
Кортикостероидтардың иммунологиялық әсерлері бар екендігі белгілі болғандықтан, таблетка түріндегі Кортимент препаратын бірге қолдану вакцинаға иммундық жауапты төмендетеді.
Жүктілік
Жүктілік кезеңінде будесонидті қолдану жөнінде деректер қандай да болсын жағымсыз құбылыстарды көрсетпейді. Пероральді түрде қоданудан кейін жүктілік нәтижесі жөнінде деректер жоқ. Жүктілік кезінде, аса қажет болған жағдайда ғана, Кортимент препаратының пайдасы қаупінен басым болған жағдайда ғана қабылдаған жөн.
Емшек емізу
Будесонид емшек сүтіне аздаған мөлшерде бөлініп шығады. Будесонидтің қаннан клиренсінің жылдамдығын ескерсек, емшек еміп жүрген нәрестеге әсері көп болмайды деп күтіледі. Дегенмен, айғақтайтын деректер жоқ. Нәресте үшін емшек емудің пайдасына және әйел үшін емдеудің пайдасына көңіл бөле отырып, емшек емізуді тоқтату немесе будесонидпен емделуді тоқтату/тоқтата тұру шешімі қабылдануы тиіс.
Ұрпақ өрбіту функциясы
Кортимент препаратының адамның ұрпақ өрбіту функциясына әсер етуі жөнінде деректер жоқ. Будесонидпен емдеуден кейін ұрпақ өрбіту функциясына әсері байқалған жоқ.
Көлік құралын немесе потенциалды қауіпті механизмдерді басқару қабілетіне дәрілік заттың ықпал ету ерекшеліктері
Кортимент препаратының автокөлікті басқару және механизмдермен жұмыс жасау қабілетіне ықпалын білу мақсатында зерттеулер жүргізілген жоқ. Көлік құралдарын басқарғанда немесе механизмдермен жұмыс жасағанда кейде бас айналу немесе қажығыштық білінуі мүмкін екендігін ескеру қажет.
Артық дозалануы
Таблетка түріндегі Кортимент препаратының жүйелік биожетімділігінің төмен болуы себепті жедел артық дозалану болады деп күтілмейді. Жедел артық дозалану жағдайында спецификалық антидоты жоқ. Емдеу демеуші және симптоматикалық емдеуден тұрады.
Шығарылу түрі және қаптамасы
Поливинилхлоридті үлбірден және алюминий фольгадан жасалған пішінді ұяшықты қаптамаға 10 таблеткадан салынған.
Пішінді 3 қаптама медициналық қолдану жөніндегі мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге картон қорапқа салынған.
Сақтау шарттары
Түпнұсқалық қаптамада 30°С-ден аспайтын температурада сақтау керек.
Балалардың қолы жетпейтін жерде сақтау керек!
Сақтау мерзімі
3 жыл
Жарамдылық мерзімі өткеннен кейін қолдануға болмайды.
Босатылу шарттары
Рецепт арқылы
Өндіруші
«Cosmo S.P.A., », ИТАЛИЯ
Via C. Colombo, 1, 20020, Lainate, Milan, Italy
Тіркеу куәлігінің ұстаушысы
«Ferring Pharmaceuticals A\S», ДАНИЯ
Kay Fiskers Plads 11, 2300 Copenhagen, Denmark
Қазақстан Республикасы аумағында тіркеуден кейін дәрілік заттың қауіпсіздігін бақылауға жауапты ұйымның атауы, мекенжайы және байланыс жасау деректері (телефон, факс, электронды пошта)
«Ферринг Фармацевтикалс С.А.» Қазақстан Республикасындағы өкілдігі
Қазақстан Республикасы, Алматы қ., 050000, Алмалы ауданы, Наурызбай батыр к-сі, 99/1 үй, 41б кеңсе.
Тел. /факс: +7(727) 311-54-47
ПЕНТАСА таблеткалар (месалазин)
Қазақстан Республикасы
Денсаулық сақтау министрлігі
Фармация комитеті Төрағасының
2017 жылғы “28” 07
№ N009631 бұйрығымен
БЕКІТІЛГЕН
Дәрілік затты медициналық қолдану жөніндегі нұсқаулық
Пентаса
Саудалық атауы
Пентаса
Халықаралық патенттелмеген атауы
Месалазин
Дәрілік түрі
Босап шығуы ұзаққа созылатын 500 мг таблеткалар
Құрамы
Бір таблетканың құрамында
белсенді зат– 500 мг месалазин,
қосымша заттар: повидон, этилцеллюлоза, магний стеараты, тальк, микрокристалды целлюлоза.
Сипаттамасы
Ақ-сұрдан бозғылт-қоңырға дейінгі түстегі теңбілді, сындыру кертігі бар және бір жақ бетінде сызықтың екі жағында «500» және «mg», екінші жақ бетінде «PENTASA» бедерленген дөңгелек таблеткалар.
Фармакотерапиялық тобы
Ішек қабынуына қарсы препараттар.
Аминосалицил қышқылы және соған ұқсас препараттар. Месалазин
АТХ коды А07ЕС02
Фармакологиялық қасиеттері
Фармакокинетикасы
Қабылдағаннан және ерігеннен кейін месалазин біртіндеп он екі елі ішектен тоқ ішекке дейін асқазан-ішек жолы (АІЖ) бойымен өткенде әр микротүйіршігінен ішек ортасының кез-келген рН мәнінде босап шығады. Препаратты ішу арқылы қабылдағаннан кейін 1 сағаттан соң микротүйіршіктер ас ішуге байланыссыз он екі елі ішекте анықталады. Дені сау еріктілерде ішектегі пассажының орташа уақыты 3–4 сағатты құрайды. Месалазин, ішектің шырышты қабығында жүйеалдылық жолмен де, бауырда жүйелі жолмен де N-ацетил-месалазинге айналады. Аздап ацетилденуі тоқ ішек бактерияларының қатысуымен жүзеге асады, соның нәтижесінде ацетил-5-аминосалицил қышқылы түзіледі. Ішу арқылы қолданғанда препараттың 30-ден 50 %-ға дейінгісі аш ішекте сіңеді. Қабылдағаннан кейін 15 минуттан соң-ақ месалазин қан плазмасында анықталады. Месалазин қан плазмасындағы ең жоғарғы концентрациясына препаратты қабылдағаннан кейін 1–4 сағаттан соң жетеді. Месалазиннің қан плазмасындағы концентрациясы біртіндеп төмендей береді және қолданғаннан кейін 12 сағаттан соң анықталмайды. Ацетил-месалазин концентрациясының қан плазмасындағы қисығы да сондай сипатта, бірақ тұтас алғанда оған жоғарырақ концентрациялары мен баяуырақ шығарылу тән. Ацетил-месалазиннің қан плазмасындағы месалазинге метаболизмдік арақатынасы тәулігіне 3 рет 500 мг және тәулігіне 3 рет 2 г қолданғаннан кейін сәйкесінше 3,5-тен 1,3-ке дейінді құрайды, бұл ацетилденуінің дозасына тәуелділігін көрсетеді. Месалазиннің қан плазмасындағы орташа тұрақты концентрациялары тәулігіне 1,5; 4 және 6 г қабылдағаннан кейін сәйкесінше 2, 8 және 12 ммоль/л құрайды. Ацетил-месалазин үшін бұл концентрациялар сәйкесінше 6, 13 және 16 ммоль/л құрайды. Месалазин мен ацетил-месалазин гематоэнцефалдық бөгет арқылы өтпейді. Месалазиннің қан плазмасы ақуыздарымен байланысуы 50 %-ға жуықты, ал ацетил-месалазиннің байланысуы — 80 %-ға жуықты құрайды. Месалазиннің қан плазмасынан жартылай шығарылу кезеңі 40 минутқа жуықты (500 мг қолданғаннан кейінгі клиренсі 18 л/сағатты құрайды), ал ацетил-месалазинде - 70 минутқа жуықты құрайды. Месалазин үнемі АІЖ арқылы өткенде босап шығатындықтан, препараттың ішу арқылы қабылдағаннан кейінгі жартылай шығарылу кезеңін анықтау мүмкін емес. Сынақ нәтижелері, месалазиннің ішу арқылы қолданғаннан кейін тұрақты концентрациясына 5 күн ішінде жететіндігін көрсетті. Месалазин мен ацетил-месалазин несеппен және нәжіспен шығарылады (несеппен көбінесе ацетил-месалазин шығарылады). Месалазиннің ішу арқылы қабылдағандағы биожетімділігі ішектің жедел қабыну аурулары кезіндегі диарея және жоғары қышқылдылық сияқты патофизиологиялық үдерістерге байланысты сәл бұзылады. Ішек перистальтикасы күшейген пациенттерде жүйелі сіңуі препараттың тәуліктік дозасының 20–25 %-ына дейін төмендейді. Бұл заттың несеппен және нәжіспен шығарылу көрсеткіштерінің артуы да ықтимал. Бауыр және бүйрек функциясының бұзылуы бар пациенттерде препараттың шығарылу жылдамдығының жеткіліксіз болуы жағымсыз нефроуытты әсерінің қаупін арттыруы мүмкін.
Фармакодинамикасы
Пентаса – босап шығуы ұзаққа созылатын таблеткалар, этилцеллюлозамен қапталған месалазиннің микротүйіршіктері түрінде келеді. Месалазин ойық жара колитін және Крон ауруын емдеу үшін пайдаланылатын сульфасалазиннің белсенді компоненті болып табылады.
Клиникалық зерттеулердің нәтижесіне сәйкес, месалазиннің емдік құндылығы пероральді және ректальді қолдану тәсілінде жүйелі әсерге қарағанда асқазан-ішек тіндерінің қабынуында жергілікті әсері жылдам болады.
Ішектің қабыну аурулары бар барлық пациенттерде лейкоциттердің жоғары көшуі, цитокиндердің аномальді өндірілуі, арахидон қышқылы метаболиттерінің жоғары өндірілуі, атап айтқанда лейкотриен В4 және ішектің қабынған тіндерінде бос радикалдардың түзілуінің күшейгені байқалады. Месалазиннің фармакологиялық әсері, цитокиндер мен лейкотриендердің өндірілуінің төмендеуі, сондай-ақ бос радикалдардың шығарылуы, in-vitro және in-vivo хемотаксис лейкоциттердің тежелуінің құрамында болады. Осы уақытқа дейін месалазиннің клиникалық тиімділігіне бұл механизмдердің қайсысы ықпал ететіні белгісіз.
Ойық жара колитінде, әсіресе патологиялық үдерісі тараған пациенттерде, ауруы >8 жыл бойы болған, анамнезінде жақын туысында ТТІО бар немесе алғашқы склероздық холангит қатар жүрген кезде тоқ ішек және тік ішек обырының (ТТІО) пайда болу қаупі жоғары. Колиттен туындаған ТТІО пайда болу қаупі, ойық жара колиті пайда болғаннан кейін 10 жыл бойы 2%, 20 жыл бойы 8% және 30 жыл бойы 18% құрайды.
9 экспериментальді емес зерттеулердің (3 топтық зерттеулерде және 6 бақылау-жағдай әдісімен зерттеулерде) салыстырмалы талдауларында ойық жара колиті бар 1,932 пациент арасында ТТІО 334 жағдайы және дисплазияның 140 жағдайы көріністелді, бұл месалазинмен ем алып жүрген пациенттерде ТТІО пайда болу қаупі 50%-ға қысқарғаны, сондай-ақ ТТІО және дисплазия үшін біріктірілген клиникалық нәтиже көрсетті. ТТІО пайда болу қаупінің қысқаруы дозалауға байланысты, бұл месалазин күніне ≥1.2 г хемопревентивті әсерінің болуына байланысты, күнделікті жазбадағы дозалануды зерттеудің салыстырмалы талдамасы дәлелдеді. Бұдан басқа хемопрофилактика месалазиннің өмірлік дозасымен (4) байланысты. Соңында месалазинмен жасалған демеуші емде ТТІО пайда болу қаупінің қысқарғаны байқалған. Экспериментальді модельдерден және пациенттер биопсиясы арқылы анықталған месалазиннің әсері препараттың ойық жаралы колит туындатқан ТТІО алдын алудағы, сондай-ақ колит туындатқан ТТІО дамуына қатысатын сигнал жолдарының қабыну үдерісімен байланысты және байланысты емес мөлшерінің төмендеуіндегі препараттың рөлін растайды.
Қолданылуы
- спецификалық емес ойық жаралы колитте
- Крон ауруында
Қолдану тәсілі және дозалары
|
Ересектер Жекелей дозалануы |
||
|
|
Ойық жара колиті |
Крон ауруы |
|
Өршу сатысы |
Месалазинді тәулігіне 1 рет 4 г-ге дейін немесе бірнеше рет қабылдау. |
Месалазинді 4 г дейін тәулігіне бірнеше рет бөліп қабылдау. |
|
Демуші ем |
Месалазиннің 2 г тәулігіне 1 рет қабылдау ұсынылады |
Месалазинді 4 г дейін тәулігіне бірнеше рет бөліп қабылдау. |
|
Балалар ( ≥ 6 жас) Жекелей дозалану. 6-18 жастағы балаларға арналған тиімділік жөнінде тек шектеулі ғана құжатталған мәліметтер бар |
|||
|
|
Ойық жаралы колит |
Крон ауруы |
|
|
Өршу сатысы |
Бастапқы доза – тәулігіне 30-50 мг/кг бірнеше рет бөліп қабылдау Ең жоғарғы доза – тәулігіне 75 мг/кг бірнеше рет бөліп қабылдау. Жалпы доза – тәулігіне 4 г көп емес (ересектерге арналған ең жоғарғы доза). |
||
|
Демуші ем |
Бастапқы доза – тәулігіне 15-30 мг/кг бірнеше рет бөліп қабылдау. Жалпы доза – тәулігіне 2 г көп емес (ересектерге арналған ұсынылатын доза). |
Бастапқы доза – тәулігіне 15-30 мг/кг бірнеше рет бөліп қабылдау. Жалпы доза – тәулігіне 4 г көп емес (ересектерге арналған ұсынылатын доза). |
|
Жалпы алғанда дене салмағы 40 кг дейінгі балаларға ересектерге арналған дозаның жартысын және дене салмағы 40 кг артық балаларға – ересектерге арналған әдеттегі дозаны қабылдау ұсынылады.
Крон ауруы бар пациенттерде 6 апта ішінде месалазиннің 4 г тәуліктік дозасына жауап болмағанда және тәулігіне 4 г месалазиннің демеуші еміне қарамастан Крон ауруы бар пациенттерде аурудың өршуі жағдайда пациенттерге басқа ем тағайындаулы тиіс.
Талетканы шайнамастан ішу керек. Таблетканы жұту оңай болу үшін тікелей қабылдаудың алдында бірнеше бөлікке бөлуге немесе 50 мл суға ерітуге болады.
Оңтайлы әсерге жету үшін препаратты тұрақты қабылдау маңызды.
Балалар. 6 жасқа дейінгі балаларға қабылдауға болмайды.
Жағымсыз әсерлері
Жиі
- бас ауыруы
- жүрек айнуы, құсу, іштің ауыруы, диарея
- тері бөртпесі (есекжемді, эритематоздық бөртпені қоса)
Сирек
- бас айналуы
- миокардит, перикардит
- метеоризм, амилаза деңгейінің жоғарылауы, панкреатит
- панколит
- дәрі-дәрмектік ауру
Өте сирек
- эозинофилия (аллергиялық реакцияның көрінісі ретінде), анемия, соның ішінде апластикалық, лейкопения (гранулоцитопенияны және нейтропенияны қоса), тромбоцитопения, агранулоцитоз, панцитопения
- аса жоғары сезімталдық реакциялары
- шеткері невропатия
- миалгия, артралгия
- ентігу, жөтел, бронх түйілуі, аллергиялық альвеолит, өкпе инфильтрациясы, өкпе эозинофилиясы, пневмония
- бауыр трансаминазалары белсенділігінің жоғарылауы, холестаз белгілері, гипербилирубинемия, гепатоуыттылық белгілері (гепатитті, холестаздық гепатитті, циррозды, бауыр жеткіліксіздігін қоса)
- жедел және созылмалы интерстициальді нефрит, нефроздық синдром, бүйрек жеткіліксіздігі, несеп түсінің өзгеруі, протеинурия, гематурия, олигурия, анурия, кристаллурия
- әлсіздік, қызыл жегіге ұқсас синдром
- алопеция
- көз жасы сұйықтығы өнімділігінің төмендеуі, паротит
- олигоспермия
- стоматит
Қолдануға болмайтын жағдайлар
- препараттың белсенді немесе қосымша компоненттеріне немесе салицилаттарға аса жоғары сезімталдық
- бауырдың және/немесе бүйректің ауыр жеткіліксіздігі
- қан жүйесінің аурулары - асқазан мен он екі елі ішектің ойық жаралы ауруы
- қан кету, геморрагиялық васкулит
- глюкоза-6-фосфатдегидрогеназа тапшылығы
- 6 жасқа дейінгі балаларға
- жүктілік және лактация кезеңі
Дәрілермен өзара әрекеттесуі
Сульфонилмочевина туындыларының гипогликемиялық әсерін, глюкокортикостероидтардың ульцерогенділігін, метотрексаттың уыттылығын күшейтеді. Фуросемидтің, спиронолактонның, сульфаниламидтердің, рифампициннің белсенділігін төмендетеді. Антикоагулянттардың әсерін күшейтеді. Урикозуриялық препараттардың (өзекшелік сөлініс блокаторларының) белсенділігін арттырады. Цианокобаламиннің сіңірілуін баяулатады. Месалазин глюкокортикоидтардың асқазанның шырышты қабығына жағымсыз әсерін әлсіретуі, дигоксиннің сіңуін төмендетуі мүмкін.
Айрықша нұсқаулар
Препаратты анамнезінде салицилаттарға (сульфасалазинге) аллергия бар пациенттерге сақтықпен қолдану қажет.
Құрысулар, абдоминальді ауру, дене температурасының жоғарылауы, қатты бас ауыруы, бөртпелер сияқты жедел симптомдар туындаған жағдайда, препаратты қабылдауды дереу тоқтату қажет.
Препаратты бауыр функциясының бұзылуы бар пациенттерге сақтықпен тағайындау керек. Қажет болса, емдеуге дейін және емдеу кезінде бауырдың AЛТ және AСТ сияқты функционалдық көрсеткіштерін бақылауға алу керек.
Препаратты бүйрек жеткіліксіздігі бар пациенттерге қолдану ұсынылмайды. Емдеу кезінде бүйрек функциясының бұзылуы месалазиннің нефроуытты әсерінен туындауы мүмкін. Бүйрек функциясын, атап айтқанда, қан сарысуындағы креатинин деңгейін ұдайы бақылап отыру қажет (әсіресе емдеудің бастапқы фазасында).
Миокардиттің, перикардиттің дамуына күдіктенгенде немесе қан құрамы өзгерген жағдайда, емдеуді тоқтату керек. Жоғарыда аталған жағымсыз реакциялардың көріністері: қан құрамының айқын өзгерістері жағдайында — қатты қанағыштық, тері астына қан кетулер, тамақтың ауыруы және қызба, перикардит немесе миокардит жағдайында — қызба, төс артының ауыруы және ентігу болуы мүмкін. Ацетилдену үдерісі баяу жүретін пациенттерде жағымсыз әсерлерінің дамуы қаупі жоғары. Несеп пен көз жасы сұйықтығының сарғыш қызыл-сары түске боялуы, жанаспалы линзалардың боялуы байқалуы мүмкін.
Егде жастағы пациенттерде қолданғанда дозасын төмендету қажет емес.
Жүктілік және лактация кезеңі
Месалазиннің плаценталық бөгет арқылы өтетіндігі белгілі. Бұл дәрінің жүктілік кезіндегі қолданылуы жөніндегі шектеулі деректер болуы мүмкін уытты әсеріне баға беруге мүмкіндік бермейді. Месалазин емшек сүтіне ана қанындағыға қарағанда төменірек концентрацияларда түседі, бұл кезде ацетил-месалазин метаболиті емшек сүтінде дәл сондай немесе жоғарырақ концентрацияларда анықталады. Аналары Пентаса препаратын қабылдаған емшектегі балаларда жағымсыз әсерлері байқалмаған, бірақ қолда бар ақпарат шектеулі. Жүктілік және бала емізу кезеңінде препаратты сақтықпен және тек, егер препарат әсерінің мүмкін болатын пайдасы ықтимал қаупінен асатын болса ғана қолдану керек.
Көлік құралдарын жүргізуге және қауіптілігі зор механизмдерді басқару қабілетіне әсер ету ерекшеліктері
Орталық жүйке жүйесі тарапынан жағымсыз әсерлерінің дамуы мүмкіндігін ескере отырып, көлік құралын немесе қауіптілігі зор механизмдерді басқарудан бас тарту керек.
Артық дозалануы
Препараттың босап шығуы ұзаққа созылатын түйіршіктер түріндегі бірегей дәрілік түрін және месалазиннің спецификалық фармакокинетикалық қасиеттерін ескере отырып, белсенді затының тек болар-болмас бөлігі ғана жүйелі әсер береді, сондықтан тіпті препараттың аса жоғары дозаларын қабылдағанда да, артық дозалануының даму симптомдарын күтпеген жөн.
Симптомдары: жүрек айнуы, құсу, гастралгия, әлсіз, ұйқышылдық.
Емі: симптоматикалық: асқазанды шаю, іш жүргізгіш дәрілерді қолдану; клиникалық жағдайға байланысты қышқыл-сілтілік теңгерімді қалпына келтіру және аралас алкалоз/ацидоз кезіндегі жоғалған электролиттердің орнын толтыру; гипергидрозда, құсуда сұйықтық көлемінің орнын толтыру; гипогликемия кезінде — глюкозаны енгізу. Бүйрек функциясын бақылау.
Шығарылу түрі және қаптамасы
Поливинилхлоридті үлбірден және алюминий фольгадан жасалған пішінді ұяшықты қаптамаға 10 таблеткадан салынған.
5 немесе 10 пішінді қаптама медицинада қолданылуы жөнінде мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге картон қаптамаға салынған.
Сақтау шарттары
Жарықтан қорғалған жерде, 25 °С-ден аспайтын температурада сақтау керек.
Балалардың қолы жетпейтін жерде сақтау керек!
Сақтау мерзімі
3 жыл
Қаптамасында көрсетілген жарамдылық мерзімі өткеннен кейін препаратты қолдануға болмайды.
Дәріханалардан босатылу шарттары
Рецепт арқылы
Өндіруші
«Ферринг Интернешнл Сентер СА», Швейцария
Chemin de la Vergognausaz 50, CH-1162 St-Prex, Switzerland
Қазақстан Республикасы аумағында тұтынушылардан өнім (тауар) сапасына қатысты шағымдарды қабылдайтын және дәрілік заттың тіркеуден кейінгі қауіпсіздігін қадағалауға жауапты ұйымның мекенжайы
Қазақстан Республикасындағы «Ферринг Фармацевтикалс С.А.» өкілдігі
Қазақстан Республикасы
Алматы қ., 050022, Наурызбай батыр к-сі, 99/1 үй, 41б кеңсе
Тел. /факс: +7(727) 311-54-47, факс: +7(727)3115287
ПЕНТАСА түйіршіктер 2 г (месалазин)
Қазақстан Республикасы
Денсаулық сақтау министрлігі
Фармация комитеті төрағасының
2018 жылғы “29” 11
№ N018359 бұйрығымен
БЕКІТІЛГЕН
Дәрілік затты медициналық қолдану жөніндегі нұсқаулық
Пентаса
Саудалық атауы
Пентаса
Халықаралық патенттелмеген атауы
Месалазин
Дәрілік түрі
Босап шығуы ұзаққа созылатын 2 г түйіршіктер
Құрамы
Бір пакеттің құрамында
белсенді зат – 2000 мг месалазин,
қосымша заттар: повидон, этилцеллюлоза.
Сипаттамасы
Ақшыл-сұр түстен ақшыл-қоңыр түске дейінгі цилиндр пішінді түйіршіктер.
Фармакотерапиялық тобы
Ас қорыту жолы және зат алмасу. Диареяға қарсы, ішекке арналған қабынуға қарсы/ микробқа қарсы препараттар. Ішекке арналған қабынуға қарсы препараттар. Аминосалицил қышқылы және ұқсас препараттар. Месалазин.
АТХ коды А07ЕС02
Фармакологиялық қасиеттері
Фармакокинетикасы
Қолданғаннан және ерігеннен кейін месалазин, асқазан ішек жолында (АІЖ) он екі елі ішектен тік ішекке дейін өткенде, қышқыл ортаның рН кез келген мәндерінде, әрбір микротүйіршіктен біртіндеп босап шығады. Препаратты пероральді түрде қолданудан кейін 1 сағаттан соң микротүйіршіктер, тамақ ішуге қарамастан, он екі елі ішектен табылады.
Переоральді түрде енгізілуден кейін Пентасаның биожетімділігі дені сау еріктілерде несепте қалпына келу деректеріне негізделген және шамамен 30% құрайды. Плазмада ең жоғары концентрациясы дозаны қабылдағаннан кейін 1-6 сағаттан соң байқалады. Месалазинді тәулігіне 1 рет (1 × 4 г / тәул.) және тәулігіне екі рет (2 × 2 г / тәул.) қабылдау 24 сағат ішінде салыстырмалы жүйелік әсерге (AUC) әкеледі және емдеудің бүкіл кезеңі ішінде препараттан месалазиннің үздіксіз босап шығатынын көрсетеді. Пероральді түрде қолданғанда тепе-тең жағдайға 5 күн емдеуден кейін жетеді.
|
|
Бір реттік доза |
Тепе-тең күй |
||
|
|
Cmax (нг/мл) |
AUC 0-24 (сағ·нг/мл) |
Cmax (нг/мл) |
AUC 0-24 (сағ· нг/мл) |
|
Месалазин |
|
|
|
|
|
2 г BID |
5103,51 |
36,456 |
6803,70 |
57,519 |
|
4 г OD |
8561,36 |
35,657 |
9742,51 |
50,742 |
|
Месалазиннің молекулалық массасы: 153,13 г/моль; Ац-месалазин: 195,17 г/моль. *BID= тәулігіне 2 рет **OD=тәулігіне 1 рет |
||||
Пероральді түрде қолданудан кейін месалазиннің өтуі және босап шығуы тамақ ішуге байланысты емес, ал сол кезде оның жүйелік әсері ұлғаюы мүмкін.
Месалазин және ацетил-месалазин гематоэнцефалдық бөгет арқылы өтпейді. Месалазиннің қан плазмасы ақуыздарымен байланысуы 50%-ға жуықты, ал ацетил-месалазиндікі 80%-ға жуықты құрайды.
Mесалазин ішектің шырышты қабығында жүйеалды түрінде, сонымен қатар бауырда жүйелік түрде, негізінен, NAT-1 жәрдемімен N-ацетил-месалазинге айналады. Аздап ацетилденуі жуан ішектегі бактериялардың қатысуымен жүзеге асырылады. Қан плазмасындағы цетил-месалазиннің месалазинге метаболизмдік арақатынасы препаратты тәулігіне 3 рет 500 мг және тәулігіне 3 рет 2 г қолданғаннан кейін, сәйкесінше, 3,5-тен 1,3-ге дейінді құрайды, бұл ацетилденудің дозаға байланысты екендігін көрсетеді. Месалазин үнемі АІЖ арқылы өткен кезде босап шығатын болғандықтан, препаратты пероральді түрде қолданудан кейін жартылай шығарылу кезеңін анықтау мүмкін емес. Препарат асқазан-ішек жолынан шығарылуға қатыспайтын болғандықтан, жартылай шығарылу кезеңі қабықшасыз месалазинді пероральді түрде немесе вена ішіне енгізуден кейін плазмадан 40 минутқа жуықты құрайтын, ацетил-месалазин үшін 70 минутты құрайтын жартылай шығарылу кезеңіне негізделген. Ішектің белсенді қабыну аурулары кезеңінде байқалатын диарея және ішектің жоғары қышқылдылығы сияқты патофизиологиялық өзгерулері, пероральді түрде қолданудан кейін ішектің шырышты қабығына месалазиннің жеткізілуіне аздаған ғана ықпалын тигізеді. Ішектік транзиті қарқынды пациенттерде тәуліктік дозаның 20-25%-ы несеппен шығарылады. Нәжіспен бірге шығарылғанда бұл тиісінше ұлғаяды.
Фармакодинамикасы
Пентаса – босап шығуы ұзаққа созылатын түйіршіктер, этилцеллюлозамен қапталған месалазиннің микротүйіршіктері болып табылады. Месалазин ойық жаралы колитті және Крон ауруын емдеу үшін пайдаланылатын сульфасалазиннің белсенді компоненті болып табылады.
Қолданудың пероральді және ректальді түрдегі тәсілінде месалазиннің емдік құндылығы, жүйелік әсеріне қарағанда, қабынған асқазан-ішек тініне жергілікті әсер етуінде болып табылады.
Месалазин қабылдаған пациенттердегі ойық жара колитінде тоқ ішектің қабынуының күрделілігі шырышты қабықтардағы месалазиннің концентрациясына кері пропорционалды деп болжам жасауға негіз беретін ақпараттар бар.
Ішектің қабыну аурулары бар барлық пациенттерде лейкоциттердің жоғары миграциясы, цитокиндердің аномальді түзілуі, арахидон қышқылы метаболиттерінің, атап айтқанда, B4 лейкотриеннің түзілуінің жоғарылауы, және ішектің қабынған тіндерінде бос радикалдардың түзілуінің күшеюі байқалады. Ішектің шырышты қабығында В каппа (NF-kB) ядролық факторлардың тежелуі және пероксис пролифераторы рецепторларымен (PPAR-гамма) белсендірілген рецепторлардың гамма-формаларының белсенділенуі сияқты механизмдердің болуы мүмкіндігіне жол берілсе де, месалазиннің әсер ету механизмі күні бүгінге дейін белгісіз. Месалазиннің in-vitro және in-vivo фармакологиялық әсері лейкоциттер хемотаксисінің тежелуінен, цитокиндер мен лейкотриенннің түзілуінің төмендеуінен, сондай-ақ бос радикалдардың шығарылуынан тұрады. Месалазиннің клиникалық тиімділігіне осы механизмдерді қайсысының көбірек ықпалын тигізетіні қазіргі таңда белгісіз.
Ойық жаралы колитте патологиялық үдерісі кең таралған пациенттерде, әсіресе ауру барысына >8 жыл болғанда, анамнезінде жақын туыстарында ТТІО бар болғанда, немесе алғашқы склероздайтын холангит қатар жүрген кезде, тоқ және тік ішек обырының (ТТІО) пайда болу қаупі жоғарылайды. Колиттің әсерінен ТТІО пайда болу қаупі ойық жаралы колит пайда болғаннан кейін 10 жыл ішінде 2%, 20 жыл ішінде 8% және 30 жыл ішінде 18% құрайды.
Ойық жаралы колитпен пациенттер арасындағы ТТІО және дисплазия жағдайлары, месалазинмен ем алып жүрген пациенттерде ТТІО пайда болу қаупі 50%-ға қысқарғанын, сондай-ақ ТТІО және дисплазия үшін біріктірілген клиникалық нәтижені көрсетті. ТТІО пайда болу қаупінің қысқаруы дозаға байланысты, осыған сәйкес месалазин күніне ≥1.2 г хемопревентивтік әсерге ие. Бұдан басқа, хемопрофилактика месалазиннің (4) өмірлік дозасымен байланысты. Ақырында, месалазинмен демеуші емді жүзеге асырудың ТТІО пайда болу қаупін қысқартатыны байқалды.
Қолданылуы
- спецификалық емес ойық жаралы колитте
- Крон ауруында
Қолдану тәсілі және дозалары
Ойық жаралы колит
Өршу фазасы
Ересектер: ең жоғары тәуліктік доза – 4 г, тәулігіне бір рет немесе 2-4 қабылдауға бөлінген, дәрігер әр адамға жекелей таңдайды.
6 жастағы және одан үлкен балалар: дозаны дәрігер әр балаға жекелей бірнеше қабылдауға, тәулігіне дене салмағының әр кг шаққанда 30-50 мг-ден бастап таңдайды. Ең жоғары тәуліктік доза - 75 мг/кг, бірақ 4 г-ден (ересектер үшін ең жоғары доза) аспайды.
Ремиссия фазасы
Ересектер: ең жоғары тәуліктік доза – 1 қабылдауға 2 г (ересектер үшін ең жоғары доза).
6 жастағы және одан үлкен балалар: дозаны дәрігер әр балаға жекелей, бірнеше қабылдауға, тәулігіне дене салмағының әр кг шаққанда 15-30 мг-ден бастап таңдайды. Ең жоғары тәуліктік доза - 2 г.
Емдеу ұзақтығын дәрігер ауру барысына байланысты әр балаға жекелей белгілейді.
Крон ауруы
Өршу фазасы
Ересектер: ең жоғары тәуліктік доза – 2-4 қабылдауға бөлінген 4 г, дәрігер әр балаға жекелей таңдайды.
6 жастағы және одан үлкен балалар: дозаны дәрігер әр балаға жекелей, бірнеше қабылдауға, тәулігіне дене салмағының әр кг шаққанда 30-50 мг-ден бастап таңдайды. Ең жоғары тәуліктік доза - 75 мг/кг, бірақ 4 г-ден аспайды.
Ремиссия фазасы
Ересектер: ең жоғары тәуліктік доза – 2-4 қабылдауға бөлінген 4 г, дәрігер әр адамға жекелей таңдайды.
6 жастағы және одан үлкен балалар: дозаны дәрігер әр балаға жекелей, бірнеше қабылдауға, тәулігіне дене салмағының әр кг шаққанда 15-30 мг-ден бастап таңдайды. Ең жоғары тәуліктік доза - 2 г.
Емдеу ұзақтығын дәрігер ауру барысына байланысты жекелей белгілейді.
Қолдану тәсілі
Пакет ішіндегісін ауызға салып, шайнамай, аздаған су немесе шырын мөлшерімен ішіп қабылдау қажет. Оңтайлы әсерге қол жеткізу үшін препаратты ұдайы қабылдау қажет.
Жағымсыз әсерлері
Жағымсыз реакцияларын бағалау жиілігі бойынша келесі жіктемеге негізделген: өте жиі (≥ 1/10), жиі (≥ 1/100-ден <1/10 дейін), жиі емес (≥ 1/1000- нан <1/100 дейін), сирек (≥ 1/10000-нан <1/1000дейін), өте сирек (<1/10000 дейін).
Белгісіз (қолда бар деректер негізінде анықтау мүмкін емес)
Жиі
- бас ауыру
- жүректің айнуы, құсу, іштің ауыруы, диарея
- тері бөртпесі (есекжемді, эритематозды бөртпені қоса)
- метеоризм
Сирек
- бас айналу
- миокардит, перикардит
- амилаза деңгейінің жоғарылауы
- панкреатит
Өте сирек
- эозинофилия (аллергиялық реакцияның көрінісі ретінде), анемия, соның ішінде апластикалық, лейкопения (гранулоцитопенияны және нейтропенияны қоса), тромбоцитопения, агранулоцитоз, панцитопения;
- аса жоғары сезімталдық реакциялары, аллергиялық экзантеманы, анафилаксиялық реакцияларды, эозинофилиямен және жүйелік көріністерімен (DRESS) дәрілік бөртпені, полиморфты эритеманы және Стивенс-Джонсон (SJS) синдромын қосқанда
- дәрі-дәрмектік қызба
- панколит
- шеткері невропатия;
- миалгия, артралгия;
- бауыр трансаминазалары деңгейінің жоғарылауы, холестаз белгілері, гипербилирубинемия, гепатоуыттылық белгілері (гепатитті, холестаздық гепатитті, циррозды, бауыр функциясының жеткіліксіздігін қоса);
- аллергиялық альвеолиттер, өкпе фиброзы (ентігуді, жөтелді, бронхтың түйілуін, өкпе эозинофилиясын, өкпенің интерстициальді ауруын, өкпе инфильтрациясын, пневмониттерді қоса)
- жедел және созылмалы интерстициальді нефрит, нефроздық синдром, бүйрек функциясының жеткіліксіздігі, несеп түсінің өзгеруі, протеинурия, гематурия, олигурия, анурия, кристаллурия;
- әлсіздік, қызыл жегіге ұқсас синдром;
- алопеция;
- көз жасы сұйықтығы өндірілуінің азаюы, паротит;
- олигоспермия;
- стоматит
Қолдануға болмайтын жағдайлар
- препараттың белсенді затына немесе қосымша заттарына немесе салицилаттарға аса жоғары сезімталдық;
- қан жүйесінің аурулары;
- асқазанның және он екі елі ішектің ойық жара ауруы;
- геморрагиялық диатез;
- бауыр және/немесе бүйрек функциясының ауыр жеткіліксіздігі;
- жүктілік және лактация кезеңі;
- 6 жасқа дейінгі балалар.
Дәрілермен өзара әрекеттесуі
Сульфонилмочевина туындыларының гипогликемиялық әсерін, глюкокортикостероидтардың ульцерогенділігін, метотрексаттің уыттылығын күшейтеді. Фуросемидтің, спиронолактонның, сульфаниламидтердің, рифампициннің белсенділігін төмендетеді. Антикоагулянттардың әсерін күшейтеді. Урикозуриялық препараттардың (өзекшелік секреция блокаторларының) тиімділігін арттырады. Цианокобаламиннің сіңуін баяулатады. Месалазин асқазанның шырышты қабығына глюкокортикоидтардың жағымсыз әсерін бәсеңдетуі мүмкін, дигоксиннің сіңуін төмендетуі мүмкін.
Айрықша нұсқаулар
Препаратты анамнезінде салицилаттарға (сульфасалазинге) аллергиясы бар пациенттерге сақтықпен қолдану қажет.
Құрысулар, абдоминальді ауыру, дене температурасының жоғарылауы, айқын бас ауыру, бөртпелер сияқты жедел симптомдар пайда болған жағдайда препарат қабылдауды дереу тоқтату қажет.
Препаратты бауыр функциясы бұзылған пациенттерге сақтықпен қолданған жөн. Қажет болғанда, емдеуге дейін және емдеу кезінде бауырдың AЛТ және AСТ сияқты функциональді көрсеткіштерін бақылау керек.
Препаратты бүйрек функциясының жеткіліксіздігі және геморрагиялық диатезі бар пациенттерге қолдану ұсынылмайды. Емдеу кезінде пациентте бүйрек функциясының бұзылуы месалазиннің нефроуыттық әсерінен туындауы мүмкін. ҚҚСП және азатиоприн сияқты, басқа белгілі нефроуытты дәрілерді бір мезгілде пайдалану, бүйректік реакциялар қаупін жоғарылатуы мүмкін. Бүйрек функциясын ұдайы бақылап отыру, атап айтқанда, қан сарысуындағы креатинин деңгейін (әсіресе емдеудің бастапқы фазасында) анықтау қажет.
Өршу сатысындағы ойық жара ауруы бар пациенттер үшін сақтық таныту ұсынылады.
Өкпе ауруы бар, атап айтқанда бронх демікпесі бар пациенттер, емдеу курсы бойы мұқият бақылауда болуы тиіс.
Миокардиттің, перикардиттің дамуына күдіктенгенде немесе қан құрамы өзгерген жағдайда емдеуді тоқтатқан жөн. Жоғарыда аталған жағымсыз реакциялардың көріністері мыналар болуы мүмкін: қан құрамында айқын өзгерулер болған жағдайда — қатты қанағыштық, тері астына қан құйылу, тамақтың ауыруы және қызба, перикардит немесе миокардит жағдайында — қызба, көкірек артының ауыруы және ентігу. Ацетилдену баяу жүретін пациенттерде жағымсыз әсерлерді даму қаупі жоғары болады. Несептің және көз жасы сұйықтығының сары-қызыл сары түске боялуы, жанаспалы линзаның боялуы байқалуы мүмкін.
Егде жастағы пациенттерге қолданғанда дозаны төмендету қажеттілігі жоқ.
Препараттың көлік құралын немесе потенциалды қауіпті механизмдерді басқару қабілетіне ықпал ету ерекшеліктері
Орталық жүйке жүйесі тарапынан жағымсыз әсерлердің дамуы мүмкін екендігін ескеріп, көлік құралын немесе потенциалды қауіпті механизмдерді басқаруды тоқтата тұрған жөн.
Артық дозалануы
Пентаса аминосалицил қышқылы болып табылатындықтан, салицилат уыттылығы симптомдары пайда болуы мүмкін. Салицилатпен артық дозалану симптомдары әдебиеттерде жақсы сипатталған.
Препараттың босап шығуы ұзаққа созылатын түйіршіктер түріндегі бірегей дәрілік түрін және месалазиннің фармакокинетикалық қасиеттерін ескерсек, белсенді заттың тек аздаған бөлігі ғана жүйелік әсер береді, сондықтан, тіпті препараттың жоғары дозаларын қолданғанның өзінде, артық дозалану симптомдарының дамуын күтпеген жөн.
Симптомдары: жүректің айнуы, құсу, гастралгия, әлсіздік, ұйқышылдық.
Емі: симптоматикалық: асқазанды шаю; іш жүргізетін дәрілерді қолдану; клиникалық жағдайға байланысты қышқыл-сілтілік теңгерімді қалпына келтіру және алкалоз/ацидоз араласқанда электролиттер жоғалуының орнын толтыру; құсуда, гипергидрозда сұйықтық көлемінің орнын толтыру; гипогликемияда — глюкозаны енгізу. Бүйрек функциясын бақылау.
Шығарылу түрі және қаптамасы
Босап шығуы ұзаққа созылатын 2 г түйіршіктер пакеттерге салынған. 60 пакеттен медициналық қолдану жөніндегі мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге картон қаптамаға салынған.
Сақтау шарттары
Түпнұсқалық қаптамасында, 25°С-ден аспайтын температурада сақтау керек.
Балалардың қолы жетпейтін жерде сақтау керек!
Сақтау мерзімі
2 жыл
Жарамдылық мерзімі өткеннен кейін қолдануға болмайды.
Дәріханалардан босатылу шарттары
Рецепт арқылы
Өндіруші
Ферринг Интернешнл Сентер СА, Швейцария
Chemin de la Vergognausaz 50, CH-1162 St-Prex, Switzerland
Тіркеу куәлігінің ұстаушысы
Ферринг Интернешнл Сентер СА, Швейцария
Қазақстан Республикасы аумағында тұтынушылардан өнім (тауар) сапасы жөніндегі шағымдарды қабылдайтын және тіркеуден кейін дәрілік заттың қауіпсіздігін бақылауға жауапты ұйымның мекенжайы (телефон, факс, электронды пошта)
«Ферринг Фармацевтикалс СА» Қазақстан Республикасындағы өкілдігі
Қазақстан Республикасы Алматы қ., 050022,
Наурызбай батыр к-сі, 99/1 үй, 41Б кеңсе
Тел.: +7(727) 311 5447, факс: +7(727) 311 5287
ПЕНТАСА ректальді суппозиторийлер (месалазин)
Қазақстан Республикасы
Денсаулық сақтау министрлігі
Фармация комитеті төрағасының
2018 жылғы «29» 11
№ N018361 бұйрығымен
БЕКІТІЛГЕН
Дәрілік затты медициналық қолдану жөніндегі нұсқаулық
Пентаса
Саудалық атауы
Пентаса
Халықаралық патенттелмеген атауы
Месалазин
Дәрілік түрі
Ректальді суппозиторийлер 1000 мг
Құрамы
1 суппозиторийдің құрамында
белсенді зат – 1000 мг месалазин,
қосымша заттар: повидон, макрогол 6000, магний стеараты, тальк.
Сипаттамасы
Ақтан сарғыш-қоңыр түске дейінгі, теңбілдері бар, сопақша пішінді суппозиторийлер.
Фармакотерапиялық тобы
Ас қорыту жолы және зат алмасу. Диареяға қарсы, ішекке арналған қабынуға қарсы/ микробқа қарсы препараттар. Ішекке арналған қабынуға қарсы препараттар. Аминосалицил қышқылы және ұқсас препараттар. Месалазин.
АТХ коды А07ЕС02
Фармакологиялық қасиеттері
Фармакокинетикасы
Месалазиннің емдік әсері негізінен оның ішектің шырышты қабығының қабынған бөлігімен жергілікті жанасуымен анықталады. Суппозиторийлерді қолдану месалазиннің тік ішектегі жоғары концентрациясының және жүйелі сіңірілуінің төмен болуын қамтамасыз етеді. Месалазин плацентарлық бөгет арқылы өтеді. Месалазин ішектің шырышты қабығында жүйеалдылық жолмен де, бауырда да жүйелі жолмен де N-ацетил-месалазинге (ацетил-месалазин) айналады. Аздап ацетилденуі тоқ ішек бактерияларының қатысуымен жүзеге асады. Месалазиннің ацетилденуі пациенттің ацетилдену фенотипімен байланыссыз екені сөзсіз. Ацетил-месалазин клиникалық және токсикологиялық тұрғыдан белсенді емес. Ректальді қолданғанда препарат баяу сіңеді, алайда қарқындылығы препараттың дозасына, құрамына және таралу дәрежесіне байланысты болады. Препаратты тұрақты түрде тәулігіне 2 г (1 г х 2) қабылдаған кездегі несептің қалпына келтірілген құрамы бойынша анықталған сіңуі 10 %-ға жуықты құрайды. Месалазиннің плазма ақуыздарымен байланысуы шамамен 50 %, ал ацетил-месалазиннің байланысуы – 80 %-ға жуықты құрайды. Месалазин мен ацетил-месалазин несеппен және нәжіспен шығарылады. Несепте негізінен ацетил-месалазин анықталады. Бауыр және бүйрек функциясының бұзылуы бар пациенттерде препараттың шығарылу жылдамдығының төмендеуі салдарынан бүйректің зақымдалу қаупі артуы мүмкін.
Фармакодинамикасы
Пентаса – месалазин сульфасалазиннің белсенді компоненті болып табылады.
Ішу арқылы және ректальді қолданғандағы месалазиннің емдік қасиеттеріне ішектің қабынған бөліктеріне жүйелі әсеріне қарағанда, көбінесе жергілікті әсері түрткі болады.
Ішектің қабыну аурулары бар пациенттерде лейкоциттер көшуі, цитокиндердің аномальді өндірілуі байқалады, арахидон қышқылы метаболиттерінің (әсіресе В4 лейкотриендердің) өндірілуі, ішектің қабынған тіндерінде бос радикалдардың түзілуі артады.
Месалазиннің фармакологиялық әсері лейкоциттер хемотаксисін бәсеңдетуден, цитокиндер мен лейкотриендер өнімдерінің мөлшерін азайтудан және бос радикалдарды бейтараптандырудан тұрады. Месалазиннің әсер ету механизмі анықталмаған.
Қолданылуы
- ойық жаралы проктитте
Қолдану тәсілі және дозалары
Ересектерге – 2 - 4 апта бойы ректальді түрде күніне бір рет 1 г (1 свеча).
Егде жастағы пациенттерге дозасын төмендетпейді.
Суппозиторийді тікелей енгізер алдында ішекті босату ұсынылады.
Суппозиторийді тік ішекке барынша терең енгізеді. Суппозиторийді ең жоғарғы емдік әсеріне қол жеткізу үшін, тік ішекте барынша ұзағырақ ұстау керек, дұрысы ұйықтар алдында пайдаланған жөн.
Егер зақымдалудың жайылған аумағы елеулі болса немесе ішу арқылы емдеуге реакция баяу жүрсе, суппозиторийлерді таблеткалармен бір мезгілде қолдануға болады. Қолдану ұзақтығын дәрігер анықтайды.
Балалар – балаларда қауіпсізділігі мен тиімділігі жөнінде қолданылуы анықталмаған.
Жағымсыз әсерлері
Жиі (≥1/100, ≤ 1/10)
- бөртпе (есекжемді, эритематозды бөртпені қоса)
Сирек (≥ 1/10 000, < 1/1000)
- бас ауыруы,
- бас айналуы,
- миокардит*, перикардит*
- амилаза деңгейінің артуы, панкреатит*
- фотосенсибилизация реакциясы**
- іштің ауыруы, диарея
- жүрек айнуы, құсу, метеоризм
Өте сирек (< 1/10 000, бірен-саран хабарламаларды қоса)
- қан талдауларының өзгеруі (апластикалық анемия, анемия, агранулоцитоз, панцитопения, нейтропения, лейкопения, тромбоцитопения) және эозинофилия (аллергиялық реакция көрінісі ретінде)
- аса жоғары сезімталдық реакциялары (аллергиялық экзантема, дәрі-дәрмектік қызба, қызыл жегі синдромы, панколит)
- шеткері нейропатия
- өкпе тарапынан аллергиялық және фиброзды реакциялар (ентігу, жөтел, аллергиялық альвеолит, өкпенің эозинофильді инфильтраты, пульмонит, бронх түйілуін қоса), өкпенің интерстициальді ауруы
- жедел панкреатит
- бауыр функциясының бұзылуы (трансаминазалар деңгейінің артуы, гепатит*, холестаздық гепатит, бауыр циррозы, бауыр жеткіліксіздігі*
- қайтымды алопеція, мультиформалы эритема, Стивенс-Джонс синдромы
- миалгия, артралгия
- бүйрек фукциясының бұзылулары*** (интерстициальді нефритті*, нефроздық синдромды қоса), несеп түсінің өзгеруі, препаратты тоқтатқаннан кейін жоғалатын бүйрек жеткіліксіздігі
- қайтымды олигиспермия
* Месалазин индукциялаған мио- және перикардиттің, панкреатиттің, нефрит және гепатиттің даму механизмі белгісіз, алайда оның шығу тегі аллергиялық болуы мүмкін.
** Фотосезімталдық: барынша күрделі реакциялар атопиялық дерматит және атопиялық экзема сияқты терінің бұрыннан болған жағдайлары бар пациенттерде байқалады.
(***) Бүйрек жеткіліксіздігі туралы хабарланған. Емдеу кезінде бүйрек дисфункциясы дамитын пациенттерде месалазин-индукциялайтын нефроуыттылыққа күдік бар.
Қолдануға болмайтын жағдайлар
- препараттың белсенді затына немесе қандай да бір қосымша затына немесе салицилаттарға аса жоғары сезімталдық
- бауырдың және/немесе бүйрек функциясының ауыр жеткіліксіздігі
- асқазан мен он екі елі ішектің ойық жаралы ауруы
- геморрагиялық диатез
- жүктілік және лактация кезеңі
- 18 жасқа дейінгі балаларға
Дәрілермен өзара әрекеттесуі
Месалазин сульфонилмочевина туындыларының гипогликемиялық әсерін, глюкокортикостероидтардың ульцерогенділігін, метотрексаттың уыттылығын күшейтеді. Фуросемидтің, спиронолактонның, сульфаниламидтердің, рифампициннің тиімділігін төмендетеді. Антикоагулянттардың әсерін күшейтеді. Урикозуриялық препараттардың (өзекшелік сөлініс блокаторларының) белсенділігін арттырады. Цианокобаламиннің сіңірілуін баяулатады. Азатиопринмен және 6-меркаптопуринмен біріктіріп емдеу миелосупрессия қаупін (лейкопения, тромбоцитопения, эритроцитопения немесе панцитопения түріндегі) арттыруы мүмкін.
Бірнеше зерттеулер, тек қана азатиопринмен емдеумен салыстырғанда, месалазин мен азатиопринді біріктіріп қолданғанда лейкопения жиі туындағанын көрсетті. Қазіргі кезде бұның себебі анықталмаған.
Лейкоциттер деңгейін жүйелі түрде бақылап отыру ұсынылады, ал тиопуриндерді дозалау режимі түзетілуі тиіс.
Айрықша нұсқаулар
Салицилаттарға аллергияның даму қаупі мүмкін болғандықтан, препаратты сульфасалазинге аллергиялық реакцияларға бейім пациенттерге сақтықпен қолдану қажет, пациент дәрігердің бақылауында болу керек.
Құрысулар, іштің қатты ауыруы, қызба, бас ауыруының күшеюі және бөртпе сияқты жақпаушылықтың жедел симптомдары пайда болған жағдайда емдеуді дереу тоқтату керек.
Бауыр функциясының жеңіл және орташа дәрежедегі бұзылуы бар пациенттерге сақтықпен қолдану керек.
Емдеу кезінде пациенттердегі бүйрек функциясының бұзылуын месалазинмен астасқан нефроуытты әсері ретінде қарастыру керек.
Басқа да белгілі нефроуытты дәрілермен, мысалы қабынуға қарсы стероидты емес дәрілермен және азатиопринмен бір мезгілде қолдану бүйрек тарапынан реакциялардың туындау қаупін арттыруы мүмкін.
Емдеу кезінде қан және несеп, бауыр функциясы параметрлері (АЛТ, АСТ) талдауларын жүргізу қажет. Талдауларды емдеуді бастар алдында, 2 аптадан соң және ары қарай 4 апта аралықпен 2-3 рет жүргізу ұсынылады. Егер зерттеу нәтижелері қалып шегінде болса, жүйелі зерттеулерді әр үш ай сайын немесе зақымдалу симптомдары пайда болған кезде жүргізуге болады.
Мочевина, сарысу креатинині деңгейі, несеп шөгіндісі мен метгемоглобин концентрациясын бақылауда ұстау ұсынылады.
Тыныс алу функциясының бұзылуы бар, әсіресе, демікпесі бар пациенттер барлық емдеу курсы бойына дәрігердің қадағалауында болуы тиіс.
Егер пациентте месалазинмен емдеу кезінде сусыздану дамитын болса, электролиттердің қалыпты деңгейлері мен сұйықтықтың теңгерімі мүмкіндігінше тез арада қалпына келтірілуі тиіс. Месалазин-индукциялайтын жүректің аса жоғары сезімталдық реакциялары (мио- және перикардит) сирек тіркелген. Күдік болғанда және реакциялар белгілері байқалған кезде мұндай емді тоқтату керек.
Дәрілік препараттың көлік құралын немесе қауіптілігі зор механизмдерді басқару қабілетіне әсер ету ерекшеліктері
Месалазин көлік құралын басқаруға немесе қауіптілігі зор механизмдермен жұмыс жасауға әсер етпейді немесе елеусіз ықпал етеді. Егер препаратпен емдеу кезінде бас айналуы байқалса, автокөлік жүргізуден бас тартқан дұрыс.
Артық дозалануы
Месалазиннің артық дозаланғаны туралы хабарламалар шектеулі. Месалазиннің дәрілік түрін ескерсек, артық дозалану қаупі онша жоғары емес.
Емі: ацидозда немесе алкалозда – қышқыл-сілтілік және электролиттік теңгерімді қалпына келтіру; сусыздануда – регидратация; гипогликемияда – глюкозаны қолдану. Диурезді арттыру үшін вена ішіне электролиттерді қосымша енгізу жүргізіледі. Арнайы антидоты жоқ.
Шығарылу түрі және қаптамасы
7 суппозиторийден пішінді ұяшықты қаптамада.
4 пішінді қаптама медициналық қолдану жөніндегі мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге картон қаптамаға салынады.
Сақтау шарттары
Жарықтан қорғалған жерде, 25 °С-ден аспайтын температурада сақтау керек.
Балалардың қолы жетпейтін жерде сақтау керек!
Сақтау мерзімі
3 жыл
Жарамдылық мерзімі өткеннен кейін қолдануға болмайды.
Дәріханалардан босатылу шарттары
Рецепт арқылы
Өндіруші
«Ферринг Интернешнл Сентер СА», Швейцария
Chemin de la Vergognausaz 50, CH-1162 St-Prex, Switzerland
Тіркеу куәлігінің ұстаушысы
«Ферринг Интернешнл Сентер СА», Швейцария
Қазақстан Республикасы аумағында тұтынушылардан дәрілік заттың сапасына қатысты шағымдарды (ұсыныстарды) қабылдайтын және дәрілік заттың тіркеуден кейінгі қауіпсіздігін қадағалауға жауапты ұйымның атауы, мекенжайы және байланыс деректері (телефон, факс, электрондық пошта)
«Ферринг Фармацевтикалс СА» Қазақстан Республикасындағы өкілдігі
050022, Қазақстан Республикасы
Алматы қ., Наурызбай батыр к-сі, 99/1 үй, 41Б кеңсе
Телефон +7 (272) 311-54-47
ПЕНТАСА ректальді cуспензия (месалазин)
Қазақстан Республикасы
Денсаулық сақтау министрлігі
Фармация комитеті
Төрағасының
2017 ж “26” 10
№ N011448 бұйрығымен
БЕКІТІЛГЕН
Дәрілік затты медициналық қолдану жөніндегі нұсқаулық
Пентаса
Саудалық атауы
Пентаса
Халықаралық патенттелмеген атауы
Месалазин
Дәрілік түрі
Ректальді cуспензия 1 г/100 мл
Құрамы:
белсенді зат: месалазин;
100 мл суспензияда 1 г месалазин бар;
қосымша заттар: динатрий эдетаты (Трилон Б); натрий метабисульфиті (Е 223); натрий ацетаты, хлорсутек қышқылы, тазартылған су.
Сипаттамасы
Ақтан ашық сары түске дейінгі cуспензия.
Фармакотерапиялық тобы
Қабынуға қарсы ішек препараттары. Аминосалицил қышқылы және ұқсас препараттар. Месалазин.
АТХ коды А07Е С02
Фармакологиялық қасиеттері
Фармакокинетикасы.
Месалазиннің емдік әсері негізінен оның ішек шырышты қабығының қабынған бөлігімен жергілікті жанасуымен белгілі болады.
Ректальді суспензияны қолдану асқазан-ішек жолының дистальді бөлімінде месалазиннің жоғары концентрациясын және төмен жүйелі сіңірілуін қамтамасыз етеді. Ректальді суспензияның төмен өрлемелі жиекті ішекте жетіп, оның шырышты қабықтарында таралуы анықталған.
Биотрансформациясы. Месалазин ішек шырышты қабығында жүйенің алдында, бауырда жүйелі жолмен N-ацетил-месалазинге (ацетил-месалазин) айналады. Аздап ацетилденуі жуан ішек бактерияларының қатысуымен жүзеге асады. Месалазиннің ацетилденуі, ықтималды түрде, пациенттің ацетилдену фенотипімен байланысты емес. Ацетил-месалазин клиникалық және токсикологиялық тұрғыда белсенді емес болып та саналады.
Сіңірілуі. Ректальді қолданғанда препарат баяу сіңеді, алайда қарқындылығы препараттың дозасына, құрамына және таралу дәрежесіне байланысты. Тұрақты күйде дені сау еріктілерде несепте ректальді cуспензияны енгізуден кейін 15-20 % жуық сіңеді.
Таралуы. Плазма ақуыздарымен месалазин байланысуы 50 % жуық, ал ацетил-месалазин 80 % жуық құрайды. Ректальді cуспензияны енгізуден кейін жүйелі сіңірілуі, ремиссия сатысындағы пациенттермен салыстырғанда, белсенді ойық жаралы колиті бар пациенттерде едәуір төмен.
Бауыр және бүйрек функциясының бұзылуы бар пациенттерде препараттың шығарылу жылдамдығының азаюы салдарынан бүйректің зақымдалу қаупі артуы мүмкін.
Фармакодинамикасы
Месалазин - ойық жаралы колит пен Крон ауруын емдеу үшін қолданылатын сульфасалазиннің белсенді компоненті.
Клиникалық зерттеулер ішу арқылы және ректальді қолдану кезінде месалазиннің емдік қасиеттеріне ішектің қабынған бөліктеріне оның жергілікті әсер етуінің, жүйелі әсеріне қарағанда, көп дәрежеде себеп болатынын көрсетеді.
Ішектің қабыну аурулары бар пациенттерде лейкоциттер көшуі, цитокиндердің аномальді өнімі, арахидон қышқылы метаболиттерінің (әсіресе, В4 лейкотриендердің) көп өндірілуі, ішектің қабынған тіндерінде бос радикалдар концентрациясының артуы байқалады.
Іn vitro және in vivo зерттеулері барысында месалазиннің фармакологиялық әсері лейкоциттер хемотаксисін бәсеңдетуден, цитокиндер мен лейкотриендер өнімін азайтудан және бос радикалдарды бейтараптандырудан тұрады. Месалазиннің әсер ету механизмі анықталмаған.
Қолданылуы
- ойық жаралы проктосигмоидит және сол жақтағы колит
Қолдану тәсілі
Ұйықтар алдында 1 клизма.
Клизманы қолданар алдында ішекті босату ұсынылады.
Клизма алюминий фольгадан жасалған пакетке салынады.
Балалар
Препарат балалар мен 18 жасқа дейінгі жасөспірімдерде қолдануға арналмаған.

Жағымсыз әсерлері
Клиникалық зерттеулер барысында бәрінен жиірек байқалған жағымсыз реакциялар: диарея, жүрек айну, іштің ауыруы, бас ауыру, құсу және бөртпе. Дәрілік затты қолданғанда кейде аса жоғары сезімталдық реакциялары және дәрі-дәрмектен болатын қызба байқалады.
Ректальді енгізуден кейін қышыну, ректальді жайсыздық және нәжіске қысылу сияқты жергілікті реакциялар болуы мүмкін.
|
Ағзалар жүйесі бойынша жіктеу |
Жиі (≥1/100, ≤ 1/10) |
Сирек (≥ 1/10 000, < 1/1000) |
Өте сирек (< 1/10 000, бірлі-жарым хабарламаларды қоса) |
Белгісіз |
|
Қан және лимфа жүйесі тарапынан |
|
|
Эозинофилия (аллергиялық реакция көрінісі ретінде), қан құрамының өзгеруі (анемия, аплазиялық анемия, лейкопения (гранулоцитопения мен нейтропенияны қоса)), тромбоцитопения, агранулоцитоз, панцитопения |
|
|
Иммундық жүйе тарапынан |
|
|
Панколит
|
Аса жоғары сезімталдық реакциялары |
|
Жүйке жүйесі тарапынан |
Бас ауыру |
Бас айналу |
Шеткері нейропатия |
|
|
Жүрек тарапынан |
|
Миокардит, перикардит |
|
|
|
Тыныс алу жүйесі тарапынан |
|
|
Өкпенің аллергиялық және фиброздық реакциялары (соның ішінде, тұншығу, жөтел, бронх түйілуі, аллергиялық альвеолит, өкпе эозинофилиясы, интерстициальді өкпе ауруы, өкпе ісінуі, пневмонит) |
|
|
Асқазан-ішек жолы тарапынан |
Диарея, іштің ауыруы, жүрек айну, құсу
|
Амилазаның жоғары деңгейі, жедел панкреатит*, метеоризм |
|
|
|
Бауыр және өт шығару жолдары тарапынан |
|
|
Бауыр ферменттерінің, холестаз параметрлерінің және билирубиннің жоғары деңгейі, гепатоуыттылық (соның ішінде гепатит*, холестаздық гепатит, цирроз, бауыр жеткіліксіздігі) |
|
|
Тері және тері асты тіндері тарапынан |
Бөрту (соның ішінде есекжем, эритемато-зды бөртпе) |
|
Шаштың түсуі |
|
|
Сүйек-бұлшықет жүйесі және дәнекер тін тарапынан |
|
|
Миалгия, артралгия, эритематоздық жегі тәрізді реакциялар |
|
|
Бүйрек және несеп шығару жүйесі тарапынан |
|
|
Бүйрек функциясының бұзылуы (соның ішінде жедел және созылмалы интерстициальдінефрит*, нефроздық синдром, бүйрек жеткіліксіздігі), несептің түссізденуі |
|
|
Жыныс ағзалары тарапынан |
|
|
Олигоспермия (қайтымды) |
|
|
Жалпы бұзылулар және енгізген жердегі бұзылулар |
|
|
|
Дәрі-дәрмектен болатын қызба |
* Месалазин қолданудан туындайтын мио- және перикардит, панкреатит, нефрит және гепатиттің даму механизмі белгісіз, бірақ шығу тегі аллергиялық болуы мүмкін.
Осы бұзылыстардың кейбірін ішек қабынуымен түсіндіруге болатынын атап өту керек.
Қолдануға болмайтын жағдайлар
- салицилаттарға, белсенді затқа немесе қосымша заттардың кез келгеніне жоғары сезімталдық
- бауыр функциясының ауыр бұзылулары немесе бүйрек жеткіліксіздігі
- балалар мен 18 жасқа дейінгі жасөспірімдерге
Дәрілермен өзара әрекеттесуі
ҚҚСП мен азатиоприн сияқты басқа белгілі нефроуытты дәрілерді бір мезгілде пайдалану бүйрек тарапынан болатын жағымсыз реакциялар қаупін арттыруы мүмкін.
Кейбір зерттеулерде Пентаса препаратымен және азатиопринмен, 6-меркаптопуринмен немесе тиогуанинмен кешенді емдеу кезінде өзара әрекеттесудің болатынын айғақтарлық миелосупрессия әсерлерінің үлкен жиілігі орын алған, алайда өзара әрекеттесу механизмі толық анықталмаған. Лейкоциттер деңгейін жүйелі бақылау және тиопуриндерді дозалау режимін тиісінше анықтау ұсынылған. Месалазиннің варфариннің антикоагуляциялық әсерін төмендету мүмкіндігінің дәлелдері мардымсыз.
Айрықша нұсқаулар
Салицилаттарға аллергияның даму қаупіне байланысты, препаратты сульфасалазинге аллергиялық реакцияларға бейімділігі бар пациенттерге сақтықпен қолдану керек.
Жедел жақпаушылық реакцияларында, мысалы, іштің шаншуында, жедел іштің ауыруында, қызба, қатты бас ауыруы мен бөртпеде емдеуді дереу тоқтату керек.
Бауыр функциясының бұзылуы бар науқастарға абайлап қолдану керек.
Дәрігердің шешімімен емделуге дейін және ем кезінде АлАТ және АсАТ сияқты бауырдың функционалдық көрсеткіштерін бақылап отыру керек.
Препарат бүйрек жеткіліксіздігі бар пациенттерге қолдануға ұсынылмайды. Бүйректің функционалдық жай-күйін (қан сарысуы креатининінің деңгейі бойынша), әсіресе, емдеудің бастапқы сатысында жүйелі бақылау керек. Ем кезінде бүйрек дисфункциясы дамыған пациенттерде месалазиннен болатын бүйректік уыттылықтан күдіктену керек. Басқа белгілі нефроуытты заттармен бір мезгілде қолданғанда бүйрек функциясын тексеру жиілігін арттыру керек.
Емделу кезінде өкпе аурулары, атап айтқанда, демікпесі бар пациенттерді мұқият тексеру керек.
Месалазин туғызған жүректік аса жоғары сезімталдық реакциялары туралы (мио- және перикардит) сирек хабарланды. Ондай симптомдар анықталғанда емдеуді дереу тоқтату керек.
Месалазин қабылдаумен байланысты күрделі қан дискразиясы туралы өте сирек хабарланды. Дәрігердің шешімімен емдеуді бастар алдында және ем кезінде толық қан талдауын жасау ұсынылады. Емдеу басталған соң 14 күн өткенде бақылау тестілерін өткізу, артынан 4 аптада бір рет мерзімділікпен тағы екі немесе үш тест өткізу ұсынылады. Егер нәтижелер қалып шегіне сәйкес болса, бақылау тестілерін әр үш ай сайын өткізу керек. Қосымша симптомдар білінгенде осы тестілер дереу өткізілу керек. Месалазинмен емделу аясында организм сусызданған жағдайда электролиттердің қалыпты деңгейі және сұйықтық теңгерімі мүмкіндігінше тезірек қалпына келтірілуі тиіс.
Балалар
Балаларды емдеу тиімділігі туралы шектеулі клиникалық деректер бар.
Жүктілік.
Месалазиннің плаценталық бөгет арқылы өтетіні белгілі. Месалазинді жүкті әйелдерге қолдану жөніндегі шектеулі деректер болуы мүмкін жағымсыз әсерлерді бағалауға мүмкіндік бермейді.
Жануарларға жүргізілген зерттеулер немесе дені сау еріктілердің қатысуымен бақыланатын зерттеулер барысында бір де бір тератогенді әсері байқалмаған.
Аналары Пентаса препаратымен емделген жаңа туған нәрестелерде қан жүйесі тарапынан бұзылулар (панцитопения, лейкопения, тромбоцитопения, анемия) туралы хабарламалар болды.
Жүктілік кезеңінде месалазинді ана үшін күтілетін пайдасы шаранаға төнетін зор қауіптен асып түссе ғана қолдануға болады.
Бала емізу кезеңі
Месалазин емшек сүтіне өтеді. Емшек сүтінде месалазин концентрациясы ана қанындағыдан төмен, ал ацетил-месалазин метаболиті емшек сүтінен дәл сондай немесе одан көп концентрацияда анықталады.
Бала емізу кезінде Пентаса препаратын қолданумен бақыланатын зерттеулер жүргізілмеген. Қазіргі уақытта бала емізетін әйелдерге месалазинді ішу арқылы қолданудың шектеулі ғана деректері бар. Аса жоғары сезімталдық реакцияларының, мысалы, жаңа туған нәрестелерде диареяның даму мүмкіндігін жоққа шығаруға болмайды.
Бала емізу кезеңінде месалазин ана үшін күтілетін пайдасы сәбиге төнетін зор қауіптен артық болса ғана қолданылады.
Автокөлікті басқару және басқа механизмдермен жұмыс істеу кезінде реакция шапшаңдығына әсер ету қабілеті
Пентаса препаратымен емдеу көлік құралдарын басқару және/немесе басқа механизмдермен істеу қабілетіне әсер етпейді.
Артық дозалануы
Месалазиннің артық дозалану жағдайлары жөнінде хабарламалар шектеулі.
Артық дозалануды емдеу: стационар жағдайларында симптоматикалық. Бүйрек функциясына мұқият мониторинг қажет.
Шығарылу түрі және қаптамасы
По 100 мл суспензии во флаконе из полиэтилена с наконечником и внутренним клапаном. По 1 флакону в пакете из алюминиевой фольги. По 5 или 7 пакетов из алюминиевой фольги и 5 или 7 полиэтиленовых пакетов в коробке из картона.
Ұштығы және ішкі клапаны бар полиэтилен құтыда 100 мл суспензиядан. Алюминий фольгадан жасалған пакетте 1 құтыдан. Алюминий фольгадан жасалған 5 немесе 7 пакеттен және 5 немесе 7 полиэтилен пакеттен картон қорапта.
Сақтау шарттары
Түпнұсқалық қаптамада 25 °С-ден аспайтын температурада сақтау керек.
Балалардың қолы жетпейтін жерде сақтау керек.
Сақтау мерзімі
3 жыл
Жарамдылық мерзімі өткеннен кейін пайдалануға болмайды.
Дәріханалардан босатылу шарттары
Рецепт арқылы
Өндіруші
«Ferring- Leciva, a.s.», Чех Республикасы
K Rybniku 475, 252 42 Jesenice u Prahу, Czech Republic.
Қазақстан Республикасы аумағында дәрілік заттың тіркеуден кейінгі қауіпсіздігін қадағалауға жауапты ұйымның атауы, мекенжайы және байланыс деректері (телефон, факс, электронды пошта)
Қазақстан Республикасындағы «Ферринг Фармацевтикалс С.А.» өкілдігі
Қазақстан Республикасы, Алматы қ., 050000, Алмалы ауданы, Наурызбай батыр к-сі, 99/1 үй, 41б кеңсе.
Тел. /факс: +7(727) 311-54-47
ПИКОПРЕП (натрий пикосульфаты, магнийдің тотығы)
Қазақстан Республикасы
Денсаулық сақтау және
әлеуметтік даму министрлігі
Mедициналық және
фармацевтикалық қызметті
бақылау комитеті Төрағасының
2017 жылғы “01” 02
№ N006500 бұйрығымен
БЕКІТІЛГЕН
Дәрілік затты медициналық қолдану жөніндегі нұсқаулық
ПИКОПРЕП
Саудалық атауы
Пикопреп
Халықаралық патенттелмеген атауы
Жоқ
Дәрілік түрі
Ішу үшін ерітінді дайындауға арналған ұнтақ 16.1г
Құрамы
1 пакеттің ішінде:
белсенді заттар: 10.0 мг натрий пикосульфаты, 3,500 г магнийдің жеңіл тотығы, 12.000 г сусыз лимон қышқылы,
қосымша заттар: түйіршіктелген калий гидрокарбонаты, натрий сахарині, құрғақ табиғи апельсин хош иістендіргіші (гуммиарабик, лактоза, аскорбин қышқылы, бутилгидроксианизол).
Сипаттамасы
Апельсиннің әлсіз иісі бар ақ түсті кристалл ұнтақ .
Дайындалған ерітінді – апельсиннің әлсіз иісі бар, жылы, ақ дерлік түсті, бұлыңғыр сұйықтық.
Фармакотерапиялық тобы
Іш жүргізетін дәрілер. Жанасу арқылы іш жүргізетін дәрілер. Басқа препараттармен біріктірілген натрий пикосульфаты.
ATХ коды A06A В58
Фармакологиялық қасиеттері
Фармакокинетикасы
Белсенді компоненттері тоқ ішекте жергілікті әсер етеді, әрі олардың ешқайсысы да елеулі мөлшерде сіңбейді.
Асқазан-ішек жолымен өту уақыты әр адамда жекелей болады, алайда ороцекальді пассаж уақыты 4-5 сағатты құрайды, ал тоқ ішек бойымен өтуї – 12-24 сағат. Пикопрептің осмостық әсері жіңішке ішекте дами бастайды, бұл препаратты қабылдағаннан кейін 2 сағат ішінде сұйықтықтың едәуір мөлшерінің ішекке шығарылуының белгісі. Препараттың ішекті қимылдатқыш әсері тек тоқ ішекте ғана дамиды және сұйықтықтың қандай мөлшерде шығарылуы мен пациенттің сұйықтықты қанша мөлшерде қосымша қабылдағанына байланысты болады. Препараттың әсері ішек босағаннан кейін толық тоқтайды, ол 6 сағаттан 18 сағатқа дейінді құрайды.
Фармакодинамикасы
Пикопреп – іш жүргізетін дәрі, препараттың әсер етуші заты іш жүргізетін әсерді стимуляциялайтын және тоқ ішекте әсер ететін натрий пикосульфаты, және тоқ ішекте ылғалды сақтаудың осмостық құбылысы есебінен іш жүргізетін әсер беретін магний цитраты болып табылады. Препараттың әсер етуі ішектің қимылдауын жақсартатын әсермен біріккен күшті жуып-шайғыш әсер түрінде білінеді, бұл радиографикалық зерттеу, колоноскопия немесе хирургиялық емшара жүргізер алдында ішекті тазалу үшін қолдануға қажет.
Қолданылуы
- рентгенологиялық зерттеулер, эндоскопиялар жүргізер алдында немесе хирургиялық араласым алдында ішекті тазалау үшін
Қолдану тәсілдері
Ауруханаға жатардан бір күн бұрын төмен калориялы диетаға көшу керек. Сусыздануға жол бермеу үшін препаратты қолдану кезінде суды көп мөлшерде ішу керек (сағатына 250 мл-ге жуық). Препарат ішке қолданылады.
Ұнтақты дайындау ережесі
Бір пакеттің ішіндегіні бөлме температурасындағы бір стақан (150 мл-ге жуық) суда ерітеді, 2-3 минут бойы араластырады және алынған ерітіндіні ішеді. Егер ерітінді қызып кетсе, ерітіндіні ішуге жарайтын температураға дейін салқындағанша күте тұру керек.
Ересектер (егде жастағы адамдарды қоса есептегенде)
Бір пакеттің ішіндегісін, жоғарыда айтылғандай, сумен сұйылтады және емшарадан бір күн бұрын кешкісін қабылдайды, қайталап қабылдау – 6-8 сағаттан кейін.
Балалар
1-2 жас: пакеттің ішіндегісінің 1/4 бөлігін таңертең және пакеттің ішіндегісінің 1/4 бөлігін күндіз;
2-4 жас: пакеттің ішіндегісінің 1/2 бөлігін таңертең және пакеттің ішіндегісінің 1/2 бөлігін күндіз;
4-9 жас: 1 пакеттің ішіндегісін таңертең және пакеттің ішіндегісінің 1/2 бөлігін күндіз;
9 жас және одан үлкен жас: дозасы ересектердегідей.
Ерітіндінің қалдығын төгіп тастайды. Дайындалған ерітіндіні сақтамайды.
Жағымсыз әсерлері
Сирек (< 1/10 000)
- асқын сезімталдық, анафилактикалық реакция
- гипонатриемия
- бас ауыру, сананың шатасуы, эпилепсия, клонико-тонустық құрысулар, қалшылдау
- жүректің айнуы, құсу, абдоминальді ауыру, диарея, прокталгия
- бөртпе (эритематозды және макулопапулярлы бөртпе), қышу, есекжем, пурпура.
Мықын астындағы ішекте афтоидты ойық жараның жеңіл қайтымды түрде дамығаны жөнінде жекелеген жағдайлардың болғаны айтылған.
Қолдануға болмайтын жағдайлар
- препараттың кез келген компонентіне асқын сезімталдықта
- жүрек қызметінің іркілген жеткіліксіздігінде
- асқазанның босауы бұзылғанда, асқазан-ішектік ойық жараларда, уытты колитте, уытты мегаколонда, ішек бітелісінде, жүрек айнығанда және құсқанда, хирургиялық араласымды қажет ететін жедел ағымды абдоминальді патологияларда, мысалы, жедел ағымды аппендицитте, сондай-ақ асқазан-ішектің бітелуі немесе тесілуі анықталғанда немесе оған күдіктенгенде
- бүйрек қызметінің жеткіліксіздігінде (қан плазмасында магнийдің жиналып қалуына байланысты)
- 1 жасқа дейінгі балаларға.
Дәрілермен өзара әрекеттесуі
Пикопреп препараты іш жүргізетін дәрі болғандықтан, ол асқазан-ішектік транзит жылдамдығын арттырады. Демек, препаратты қабылдау ішу арқылы қабылданатын басқа дәрілік препараттардың (мысалы, эпилепсияға қарсы және диабетке қарсы препараттардың, контрацептивтердің және антибиотиктердің) сіңуін өзгертуі мүмкін.
Пикопреп препаратының тиімділігі ішектің ішіндегі заттардың көлемін ұлғайтатын іш жүргізетін дәрілермен бір мезгілде қабылдаған кезде төмендейді.
Гипокалиемияны тудыратын препараттарды (диуретиктер немесе кортикостероидтар, сондай-ақ гипокалиемияның ерекше қаупінің дамуына байланысты қабылданатын препараттар сияқты, мысалы, жүрек гликозидтерін) қабылдап жүрген пациенттерде препаратты қолданғанда сақ болған жөн. Пикопрепті қабынуға қарсы стероидты емес препараттарды немесе антидиуретикалық гормонның талапқа сай емес секрециясы синдромын индукциялайтын препараттарды, мысалы, үшциклдік антидепрессанттарды, серотонинді кері ұстап қалатын селективтік тежегіштерді, антипсихотикалық препараттарды және карбамазепин препараттарын қабылдап жүрген пациенттерге тағайындағанда сақ болған жөн, өйткені олар суды ұстап қалу және/немесе электролиттер тепе-теңдігінің бұзылу қаупін арттыруы мүмкін.
Айрықша нұсқаулар
Препаратты асқазан-ішек жолына жуық арада хирургиялық емшара жүргізгеннен кейін, сондай-ақ бүйрек қызметі бұзылған, жүрек аурулары немесе ішектің қабыну аурулары бар пациенттерге аса сақтықпен қолданған жөн.
Су және электролит тепе-теңдігіне ықпалын тигізуі мүмкін препараттарды, мысалы, диуретиктерді, кортикостероидтарды, литийді қолданып жүрген пациенттерге препаратты абайлап қолданған жөн.
Пикопреп препараты ішу арқылы жүйелі қолдануға арналған дәрілік препараттардың сіңуін өзгерте алатын болғандықтан, оны осыған ұқсас жағдайларда абайлап қолданған жөн; өйткені бұрын эпилепсияға қарсы, эпилепсияны ойдағыдай бақылауға мүмкіндік берген, препараттарды қабылдап жүрген пациенттерде конвульсия ұстамалары жөнінде жекелеген мәлімдемелер алынды.
Суды және электролиттерді жеткіліксіз ішу олардың, әсіресе әлсіз пациенттерде, клиникалық тұрғыдан маңызды тапшы болуына әкеп соқтырады. Сондықтан егде жастағы пациенттер және әлсіз пациенттер, сондай-ақ гипокалиемия қаупі бар пациенттер медициналық бақылауда болуы тиіс. Гипонатриемия белгілері немесе симптомдары бар пациенттерде сұйықтықтың және электролиттердің тепе-теңдігін қалпына келтіру үшін оны тез түзететін шаралар жүргізу қажет етілуі мүмкін. Сұйықтықты жеткілікті мөлшерде ішкен жөн.
Ішекті тазалау кезеңі 24 сағаттан аспауы тиіс, өйткені өте ұзақ емшара судың немесе электролиттің тепе-теңдігінің бұзылу қаупін арттыруы мүмкін.
Препаратта лактоза бар, сондықтан оны лактоза жақпайтын пациенттерге қолданбаған жөн.
Препарат әдеттегідей іш жүргізетін дәрілер ретінде қолдануға арналмаған.
Балалар
Препаратты балаларға 1 жасынан бастап аурухана жағдайында дәрігердің бақылауымен қолданады.
Жүктілік және лактація кезеңінде қолданылуы
Пикопреп препаратын жүктілік кезеңінде қолданудың клиникалық тәжірибесі шектеулі, сондықтан оны әсіресе жүктіліктің алғашқы триместрінде абайлап қолданған жөн.
Натрий пикосульфаты, магний цитраты емшек сүтіне бөлініп шықпайды.
Дәрілік заттың көлікті басқару және қозғалыстағы механизмдермен қызмет көрсету қабілетіне ықпал ету ерекшеліктері
Конвульсияның, құрысудың немесе сананың шатасуының пайда болуы мүмкін екендігін ескеріп, препаратты қолдану кезеңінде автокөлікті басқаруды немесе басқа да механизмдермен жұмыс жасауды тоқтата тұрған жөн.
Артық дозаланғанда
Симптомдары: профуздық диарея даму мүмкін.
Емдеу: жалпы демеуші ем жүргізу және сұйықтықтың мол мөлшерде ішілуін қамтамасыз ету
Шығарылу түрі және қаптамасы
16.1 г препарат төрт қабатты пакетке салынады, 2 пакеттен медициналық қолдану жөніндегі мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге картон қорапқа салынған.
Сақтау шарттары
25°С-ден аспайтын температурада , түпнұсқалық қаптамада сақтау керек.
Балалардың қолы жетпейтін жерде сақтау керек!
Сақтау мерзімі
3 жыл
Еріткеннен кейін дайын ерітіндіні бірден пайдалану керек.
Босатылу шарттары
Рецепт арқылы
Өндіруші
«Ferring Pharmaceutical Compani Limited», ҚЫТАЙ
No.6 HuiLing Lu (Ferring Road), National Health Technology Park, Zhongshan City, Guangdong Province
Тіркеу куәлігінің иесі
«Ферринг ГмбХ», Германия
Wittland 11, 24109 Kiel, Germany
Қазақстан Республикасы аумағында тұтынушылардан өнімнің (тауардың) сапасына қатысты шағымдарды қабылдайтын және дәрілік заттың тіркеуден кейінгі қауіпсіздігін қадағалауға жауапты ұйымның мекенжайы
ҚР-дағы «Ферринг Фармацевтикалс С.А.» өкілдігі
Қазақстан Республикасы
Алматы қ., 050059
Әл-Фараби даңғ., 7 блок 5а, 131 кеңсе
«Нұрлы Тау» Бизнес Орталығы
Тел.: +7(727) 311 5447
РЕМЕСТИП (терлипрессин)
Қазақстан Республикасы
Денсаулық сақтау министрлігі
Фармация комитеті Төрағасының
2017 жылғы “05” 12
№ N012176, N012177 бұйрығымен
БЕКІТІЛГЕН
Дәрілік затты медициналық қолдану жөніндегі нұсқаулық
Реместип
Саудалық атауы
Реместип
Халықаралық патенттелмеген атауы
Терлипрессин
Дәрілік түрі
Инъекцияға арналған 0.1 мг/мл 2 мл және 10 мл ерітінді
Құрамы
1 мл препараттың құрамында
белсенді зат – 0,1 мг терлипрессин (бос негіз),
қосымша заттар: натрий хлориді, сірке қышқылы, натрий ацетатының үшгидраты, инъекцияға арналған су.
Сипаттамасы
Мөлдір түссіз ерітінді
Фармакотерапиялық тобы
Жүйелі қолдануға арналған гормональді препараттары. Гипоталамус- гипофизарлы гормондар және оның аналогтары. Гипофиздің артқы бөлігінің гормондары. Вазопрессин және оның аналогтары. Терлипрессин.
АТХ коды H01BA04.
Фармакологиялық қасиеттері
Фармакокинетикасы
Терлипрессиннің тегіс бұлшықетке қатынасы белсенді емес, бірақ ол ферменттік ыдырау нәтижесінде түзілетін фармакологиялық тұрғыдан белсенді субстанция үшін химиялық қор болып табылады. Бұл әсері лизин-вазопрессиннің әсеріне қарағанда баяуырақ дамиды, бірақ едәуір ұзақ әсер етеді. Лизин-вазопрессин әдетте бауырда, бүйректерде және басқа да тіндерде биотрансформацияға ұшырайды. Жартылай шығарылу кезеңі 40 минутты құрайды, метаболизмдік клиренсі минутына – 9 мл/кг, таралу көлемі – 0,5 л/кг. Қанда лизин-вазопрессиннің күтілетін концентрациясы терлипрессинді енгізгеннен кейін шамамен 30 минуттан соң байқалады. Ең жоғары концентрация 60 және 120 минут арасындағы кезеңде байқалады.
Фармакодинамикасы
Реместип - терлипрессин (N-триглицил-8-лизин-вазопрессин), гипофиздің артқы бөлігінің табиғи гормоны вазопрессиннің синтетикалық аналогы болып табылады, одан 8-ші позициясында аргининнің орны лизинге алмастырылуымен, сондай-ақ үш глицинді қалдық цистеиннің терминальді амин тобына қосылуымен ерекшеленеді. Терлипрессиннің фармакологиялық әсері субстанцияның ферменттік ыдырауының нәтижесінде түзілген оның ерекше әсерінің басылуы болып табылады. Терлипрессиннің елеулі қасиеттері айқын вазоконстрикторлы және геморройға қарсы әсері болып табылады. Осыған қатысты өте айқын әсері ішкі ағзалардың паренхимасында қан айналымының төмендеуі болып табылады, соның нәтижесінде бауырдағы қан ағысы және қақпалық вена жүйесіндегі қысым төмендейді.
Фармакодинамикалық зерттеулер терлипрессиннің пептидтер сияқты көбіне ішкі ағзалардың паренхимасында артериолалардың және венулалардың түйілуін, өңеш қабырғасының тегіс бұлшықеттерінің тартылуын, барлық ішектің тонусы мен жиырылуын тудыратынын көрсетті. Терлипрессин жатырдың тегіс бұлшықеттерін, соның ішінде жүктілік болмаған кезде, стимуляциялайды. Препараттың ең жоғары белсенділігі ішкі ағзаларда және теріде білінді. Терлипрессиннің диурезге қарсы әсерінің клиникалық біліністері байқалған жоқ.
Қолданылуы
- асқазан-ішектік қан кетулер (өңеш веналарынан қан кету, асқазан мен 12 елі ішектің ойық жараларынан қан кету)
- несеп жолдарынан қан кету
- жыныс жолдарынан қан кету (атқаратын қызметінің бұзылуларымен немесе басқа да себептермен, босанумен, абортпен байланысты жатырдан қан кету)
- құрсақ қуысындағы және кіші жамбастағы ағзаларға жасалған хирургиялық араласымдармен байланысты қан кетулерде
- гинекологиялық араласым кезінде (жатыр мойнына) жергілікті қолдану үшін.
Қолдану тәсілі және дозалары
Өңештің варикозды түрде кеңейген веналарынан қан кету: 3 – 5 күн бойы әрбір 4-6 сағат сайын 1,0 мг. Қан кетудің қайталануының профилактикасы үшін емді қанды тоқтатқаннан кейін 24 сағаттан 48 сағатқа дейін жалғастырған жөн. Препарат вена ішіне болюсті түрде немесе қысқа уақыттық инфузиялар түрінде қолданылады.
Асқазан-ішектік қан кетулердің басқа түрлері:
әрбір 4-6 сағат сайын вена ішіне 1,0 мг.
Препарат сондай-ақ, егер асқазан-ішек жолының жоғарғы бөлімдерінен қанның кеткеніне күдік бар болса, хирургиялық араласымнан тыс алғашқы жәрдем ретінде қолданылуы мүмкін.
Несепжыныс жолдарынан қан кету: қан плазмасында және тіндерде эндопептидаза белсенділігінің айырмашылықтарын ескеріп, дозалау аралығын барынша ауқымды ету – 4-6 сағаттық аралықпен вена ішіне 0,2 мг-нан 1,0 мг-ға дейін.
Жасөспірімдік жатырлық қан кетулерде вена ішіне дене салмағының әр кг-на шаққанда 5 мкг-нан 20 мкг-ға дейінгі доза ұсынылады.
Балаларда ішкі ағзалардан қан кетулер: қан кету толық тоқтағанша әрбір 4 – 8 сағат сайын дене салмағының әр кг-на шаққанда 8 мкг-нан 20 мкг-ға дейін. Өңештің склерозданған варикозды түйіндерінде вена ішіне болюсті түрде 20 мкг/кг доза бір рет енгізуге тағайындалады.
Гинекологиялық араласымдарда жергілікті қолдану: 0,4 мг-ды 0,9% натрий хлориді ерітіндісімен 10 мл көлемге дейін сұйылтады және интрацервикальді немесе парацервикальді түрде енгізеді. Препараттың әсері 5 – 10 минуттан кейін байқалады. Қажет болған кезде доза арттырылуы немесе қайтадан тағайындалуы мүмкін.
Жағымсыз әсерлері
Жиі (≥1/100 <1/10 дейін)
- бас ауыру
- бозару, артериялық қысымның жоғарылауы, брадикардия, жүрек жеткіліксіздігі, миокард инфаркті
- жүректің айнуы, іштің ауыруы, ішек перистальтикасының ішектің түйілуіне дейін күшеюі, диарея
Сирек (≥1/10000 <1/1000 дейін)
- ентігу
Өте сирек (<1\10000)
- инъекция жасалған жерде фокальді некроз.
Қолдануға болмайтын жағдайлар
- терлипрессинге және қосымша заттарға аса жоғары сезімталдық
- жүктіліктің бірінші триместрінде, өмірлік көрсетілімдерін қоспағанда
- жүкті әйелдер гестозы
- эпилепсия.
Дәрілермен өзара әрекеттесуі
Препаратты басқа дәрілік заттармен араластырмаған жөн.
Окситоцинмен және метилэргометринмен бір мезгілде қолданған кезде миометрий тонусына вазоконстрикторлы және стимуляциялаушы әсері күшейеді. Реместип портальді гипертензияны төмендетуге қатысты селективті емес бета-адренобөгегіштердің әсерін потенциялайды. Жүректің жиырылу жиілігін төмендететін препараттармен қатарластыра қолдану ауыр брадикардияны тудыруы мүмкін.
Айрықша нұсқаулар
Препаратты егде жастағы пациенттерге, ЖИА, ауыр артериялық ауыр гипертензиясы, жүрек аритмиялары, бронх демікпесі бар науқастарға абайлап қолданған жөн.
Реместиппен емдеу үдерісінде, егер препарат жоғары дозаларда (0,8 мг және одан астам) тағайындалса, әсіресе ауыр гипертензиясы, жүрек аурулары бар пациенттерде, сондай-ақ егде жастағы адамдарда артериялық қысымды, тамырдың соғуын, сұйықтықтың тепе-теңдігін мұқият бақылау қажет.
Реместип айналымдағы қан көлемінің (АҚК) тапшылығы бар пациенттерде қанның орнын басатын дәрі болып табылмайды. Терлипрессинді қолданғаннан кейін фокальді некроздар эпизодтық түрде байқалатын болғандықтан, бұлшықет ішіне енгізуге жол бермеу керек және сұйылтылмаған 0,5 мг және одан астам дозалардағы препаратты қолданбаған жөн.
Жүктілік және лактация кезеңі
Терлипрессин миометрий белсенділігін стимуляциялайды және жатырлық қан ағысын төмендетеді. Препараттың ұрпақ өрбіту функциясына ықпалы жөнінде жүргізілген зерттеулер терлипрессиннің жоғары дозалары аборт санының немесе шарананың ерте өлімінен кейінгі аборт санының артуына әкелетіндігін айғақтайды. Кейбір жағдайларда тірі туылған шарананың дене салмағының аз және іштен туа болатын кемістіктер санының көп болатындығы анықталды.
Препаратты, өмірлік көрсетіліммен байланысты жағдайларды қоспағанда, жүктіліктің бірінші триместрінде қолдануға болмайды. Жүктіліктің басқа триместрлерінде Реместип ана үшін күтілетін пайдасы/ шарана үшін ықтимал қаупі арақатынасына баға берілгеннен кейін ғана тағайындалады.
Препараттың емшек сүтімен бірге бөлініп шығуы жөнінде мәліметтер жеткілікті емес. Нәрестенің асқазан-ішек жолында өзгермеген пептидтің елеулі мөлшерде сіңуі мүмкін екендігі екіталай.
Балалар
Препаратты ұсынылған сызбаға сәйкес қолданады («Қолдану тәсілі және дозалары»).
Көлікті немесе қауіптілігі зор механизмдерді басқару қабілетіне ықпал ету ерекшеліктері
Препараттың жағымсыз әсерлерін ескеріп, көлікті немесе қауіптілігі зор механизмдерді басқарған кезде сақ болған жөн.
Артық дозалануы
Симптомдары: дозаны 2,0 мг астамға арттырған кезде 4 сағат ішінде жүйелік қан ағысына күрделі жағымсыз әсерлердің қаупі артады.
Емі: препаратпен емдеу аясында артериялық гипертензия дамыған кезде жағдайды бақылау үшін клонидинді немесе симпатолитиктерді қолданған жөн. Брадикардияны басу үшін атропинді қолданған жөн.
Шығарылу түрі және қаптамасы
Түссіз, мөлдір шыныдан жасалған ампулаларға препарат 2 мл-ден немесе 10 мл-ден салынған.
5 ампуладан медициналық қолдану жөніндегі мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге картон қорапқа салынған.
Сақтау шарттары
Тоңазытқышта 2 0C-ден - 8 0C-ге дейінгі температурада түпнұсқалық қаптамасында сақтау керек. Мұздатып қатыруға болмайды.
Балалардың қолы жетпейтін жерде сақтау керек!
Сақтау мерзімі
2 жыл
Қаптамасында көрсетілген жарамдылық мерзімі өткеннен кейін қолдануға болмайды.
Дәріханадан босатылу шарттары
Рецепт арқылы
Өндіруші
«Зентива к.с.», Чех Республикасы
U Kabelovny 130 102 37 Praha 10 - Dolni Mecholupy, Czech Republic
Тіркеу куәлігінің иесі
«Ферринг-Лечива а.с.», Чех Республикасы
K Rybníku 475, 252 42 Jesenice u Prahy, Czech Republic
Қазақстан Республикасы аумағында дәрілік заттың тіркеуден кейінгі қауіпсіздігін қадағалауға жауапты ұйымның атауы, мекенжайы және байланыс деректері (телефон, факс, электронды пошта)
Қазақстан Республикасындағы «Ферринг Фармацевтикалс С.А.» өкілдігі
Қазақстан Республикасы
Алматы қ., 050000, Алмалы ауданы, Наурызбай батыр к-сі, 99/1 үй, 41б кеңсе
Тел. /факс: +7(727) 311-54-47






